Sífilis Adquirida: O Que Você Precisa Saber
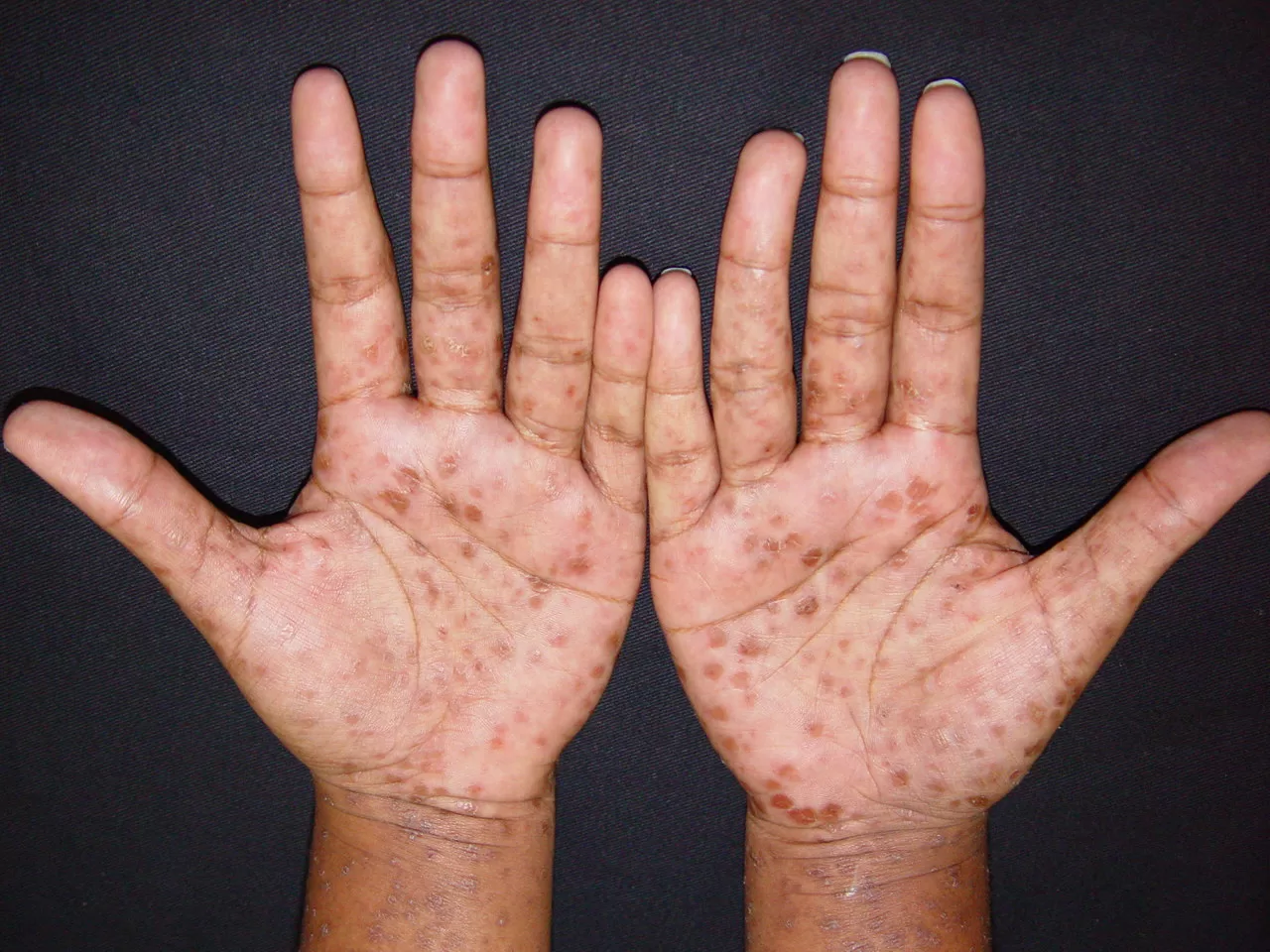
A sífilis é uma infecção transmitida, principalmente, através de contato sexual, causada pela bactéria Treponema pallidum. Com uma vasta gama de manifestações clínicas, é frequentemente referida como “a grande imitadora” devido à sua capacidade de simular muitas doenças da pele.
Nos últimos anos, observamos um crescimento preocupante na incidência da sífilis, principalmente entre homens que têm relações sexuais com homens. Este aumento é em grande parte devido à transmissão da doença nas fases primária e secundária.
Além disso, a incidência entre mulheres e indivíduos heterossexuais também tem aumentado, estando muitas vezes associada ao uso de drogas injetáveis e práticas sexuais promíscuas.
Com o aumento da incidência da sífilis em mulheres, também temos visto um crescimento dos casos de sífilis congênita. Vamos abordar este tópico em detalhe em um artigo separado.
Um exame detalhado da pele é fundamental para identificar a sífilis em suas fases iniciais. Detectar e tratar a doença precocemente é essencial para prevenir a transmissão e evitar complicações a longo prazo, incluindo lesões destrutivas e sequelas da fase avançada da doença.
Neste artigo, discutiremos a evolução da sífilis ao longo das últimas décadas, seus principais métodos de transmissão, as diferentes manifestações clínicas e as abordagens terapêuticas recomendadas.
Tendências na Incidência da Sífilis ao Longo dos Anos
A sífilis tem mostrado flutuações em sua incidência ao longo da história. Observou-se um pico epidêmico em 1990, e, a partir de 2001, o número de casos começou a crescer novamente.
Grupos de Maior Vulnerabilidade
Os jovens, especialmente entre 15 e 25 anos, são mais afetados devido à maior atividade sexual e comportamentos promíscuos.
Além disso, grupos sociais com menor escolaridade também apresentam maior vulnerabilidade.
Outros grupos de risco incluem marinheiros, soldados em combate, turistas, profissionais do sexo e homens que têm relações sexuais com homens.
Fatores de Risco Aumentado
O aumento na incidência da sífilis pode ser atribuído a várias razões:
- Início precoce da atividade sexual, frequentemente associado à confiança em métodos contraceptivos para prevenção da gravidez.
- Prolongamento da atividade sexual em homens devido ao uso de medicamentos para disfunção erétil.
- Deslocamentos frequentes, como turismo e movimentações militares, dificultam o rastreio dos infectados.
- A confiança excessiva em antibióticos específicos, que pode levar a um comportamento sexual mais arriscado.
- Uma formação médica insuficiente no que diz respeito a doenças sexualmente transmissíveis, resultando em diagnósticos tardios e maior transmissão.
Estatísticas Recentes
Desde o início do século XXI, notou-se um aumento expressivo da doença em homens, especialmente ligado à transmissão entre homens que têm relações sexuais com homens, representando 54% dos casos nas fases primária e secundária.
Mulheres também mostraram um aumento na incidência, frequentemente associado ao uso de drogas injetáveis. Concomitantemente, houve um crescimento nos casos entre homens usuários de drogas relacionado à transmissão heterossexual.
Devido ao crescimento dos casos em mulheres, a sífilis congênita também tem mostrado tendência de aumento.
Além disso, é preocupante o alto índice de coinfecção com HIV em homens homossexuais, nas fases iniciais da sífilis, atingindo 42%.
Desde 2009, houve um crescimento nos casos de sífilis tardia, relacionado ao aumento da doença em sua fase precoce, observada no final dos anos 80 e início dos anos 90.
Transmissão da Sífilis: Entenda os Riscos e Proteja-se
A sífilis é causada pela bactéria Treponema pallidum, uma bactéria delicada e sensível ao calor, com dificuldade de sobreviver fora do corpo humano.
A transmissão da sífilis acontece de diversas maneiras:
- Relações Sexuais: É a via mais comum de contaminação. Mesmo que a bactéria possa penetrar a pele ou mucosas intactas, ela tem mais facilidade de entrar através de lesões ou feridas abertas.
- Via Placentária: O que resulta na sífilis congênita, afetando o feto.
- Transfusão de Sangue: A transmissão por doação de sangue é rara, graças à rigorosa triagem de doadores e exames específicos.
- Contaminação Acidental: Profissionais de saúde, como médicos, dentistas e técnicos de laboratório, podem ser contaminados ao manusear lesões infectadas.
Após a entrada da bactéria no corpo, ela se multiplica rapidamente no local de inoculação e, em poucas horas, espalha-se por todo o organismo através dos sistemas linfático e sanguíneo.
Mesmo quando a lesão é visível apenas no ponto de entrada, a bactéria já pode ter se disseminado para todo o corpo.
A Resposta Imunológica do Corpo Humano
Não temos imunidade natural contra a sífilis, o que nos torna suscetíveis à contaminação.
Na fase inicial da doença, o corpo ainda não possui a capacidade de combater efetivamente a bactéria.
A imunidade só é adquirida nas fases mais avançadas da doença, tornando possível a reinfecção nas fases primária e secundária, mas não nas fases mais tardias.
A natureza prolongada da sífilis se deve à demora na geração de uma resposta imunológica efetiva, liderada pelos linfócitos T.
Contudo, na maioria dos casos, a doença eventualmente evolui para a cura.
Entendendo a Classificação da Sífilis: Diferentes Estágios da Doença
Baseando-se na duração e evolução da doença, a sífilis é categorizada da seguinte maneira:
- Sífilis Congênita: Adquirida durante a gestação, transmitida da mãe para o feto, via placentária.
- Sífilis Adquirida: Este tipo é posteriormente subdividido em:
- Sífilis Recente (até 1 ano de duração): Engloba as fases primária, secundária e a latente recente. A fase latente recente, também conhecida como” fase do silêncio da doença”, surge após a fase secundária e só pode ser identificada através de exame no sangue.
- Sífilis Tardia (mais de 1 ano de duração): Esta fase compreende a sífilis terciária cutânea, cardiovascular, nervosa, visceral e a latente tardia.
Por que a classificação da sífilis é importante?
Do ponto de vista clínico e epidemiológico, entender a fase da sífilis é crucial. A sífilis recente tem uma maior probabilidade de transmissão, mas é menos propensa a afetar outros órgãos, em especial o sistema nervoso central, quando comparada à sífilis tardia.
Manifestações da Sífilis: Entendendo a Fase Primária
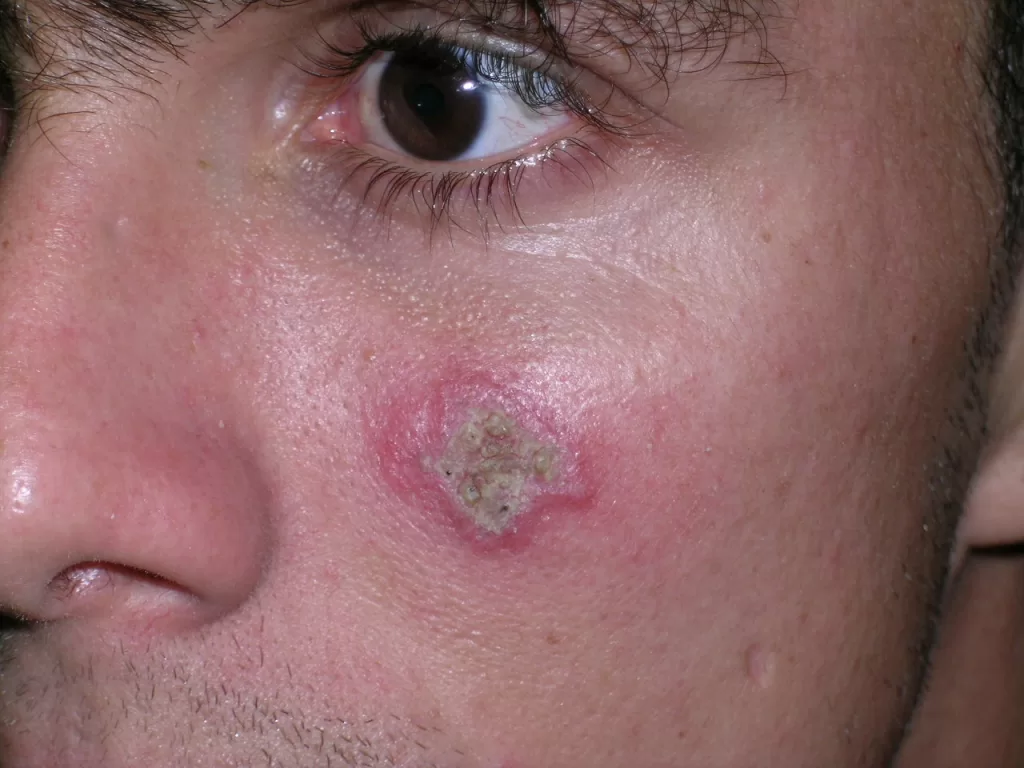
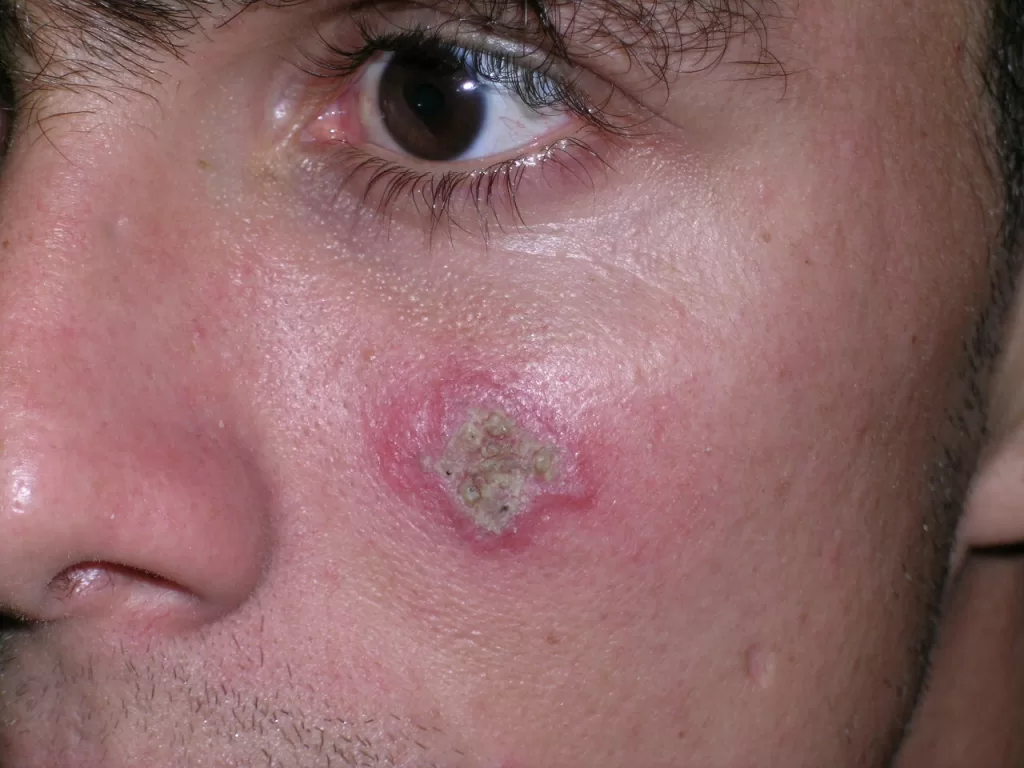
A primeira manifestação da sífilis surge, em média, 3 semanas após a infecção, marcada pelo surgimento do cancro sifilítico, que se localiza no ponto de inoculação da bactéria.
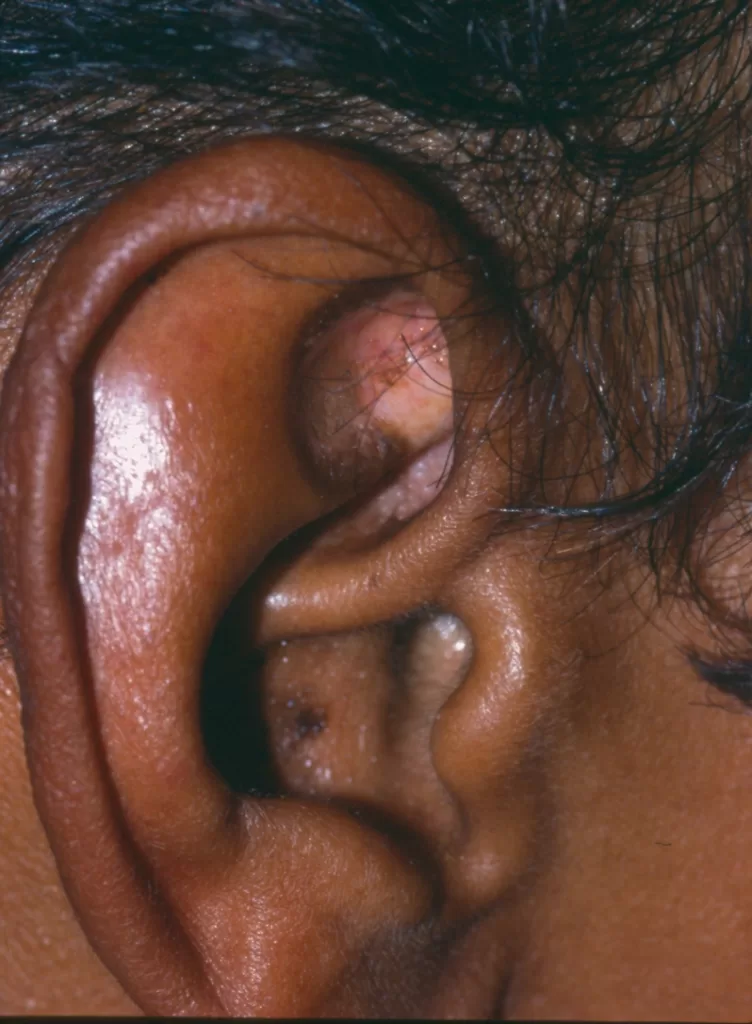
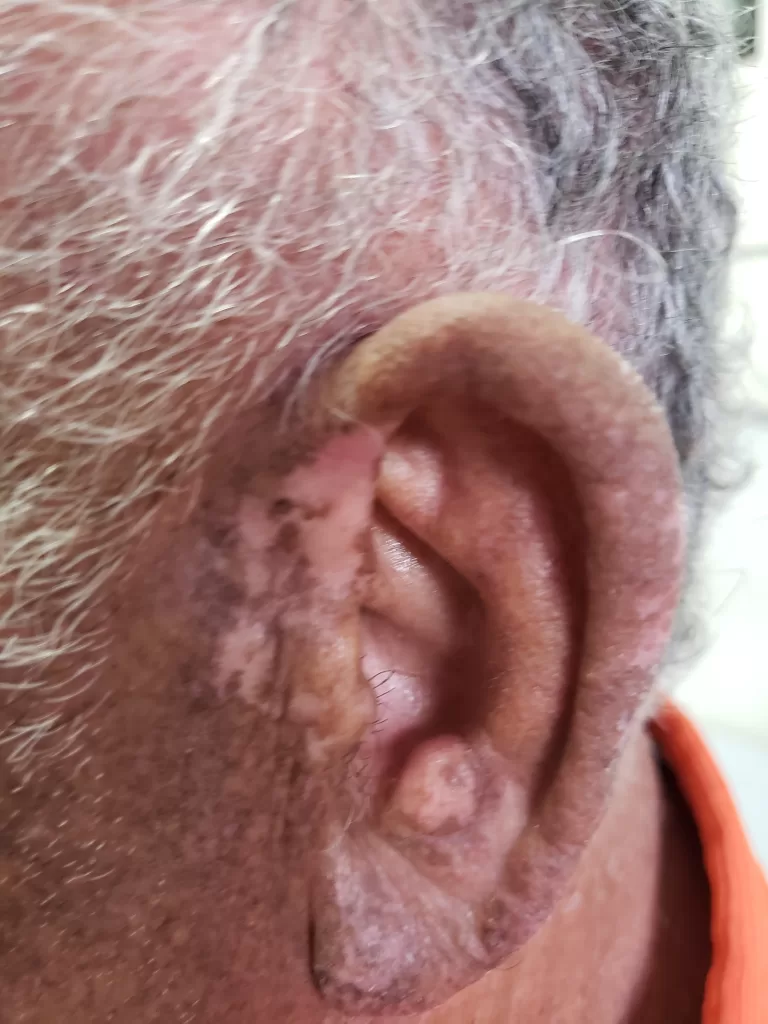
Características do Cancro Sifilítico:
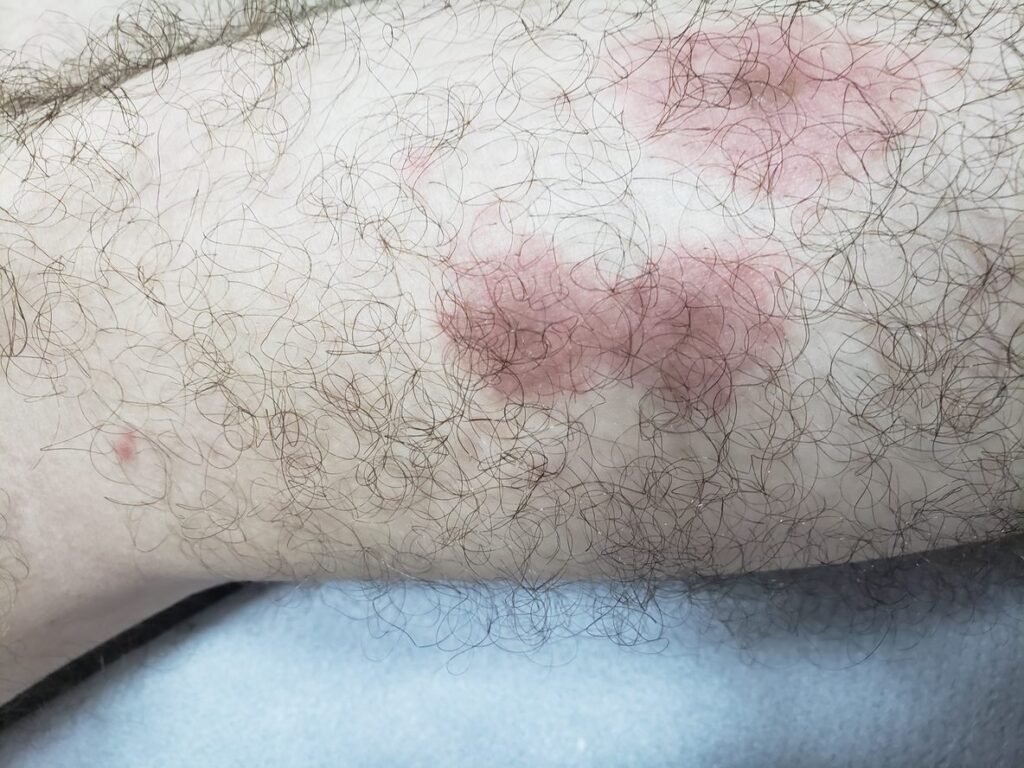
- Início: Surge como uma pápula(“carocinho”), transformando-se rapidamente em ferida.
- Aparência: Ferida única, redonda ou ovalada, de cor avermelhada e sem pus. Apresenta líquido com alta concentração da bactéria.
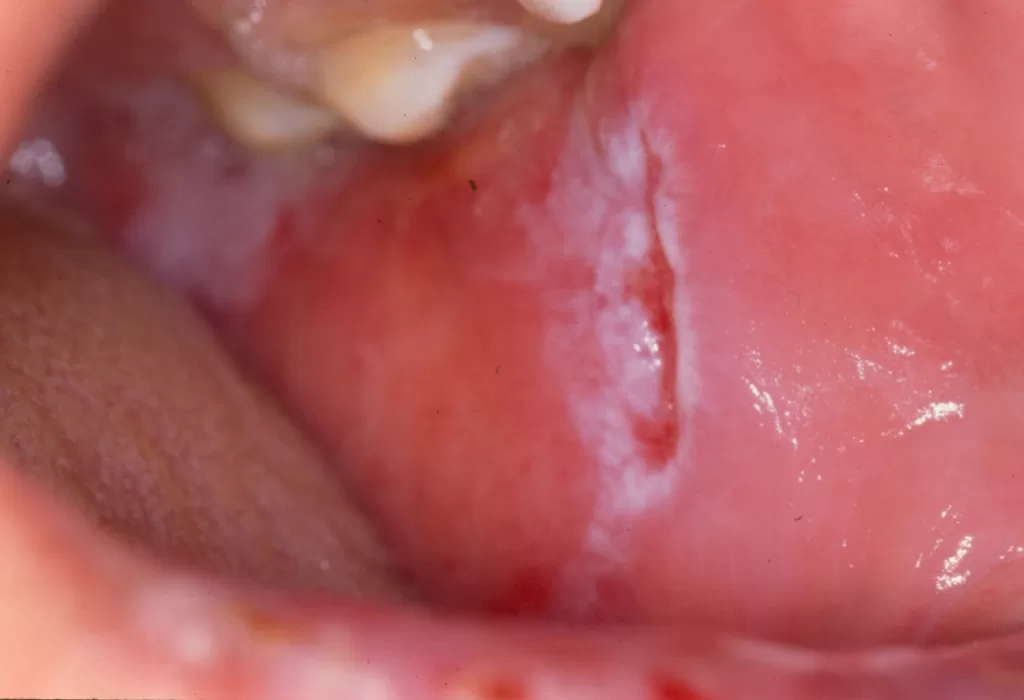
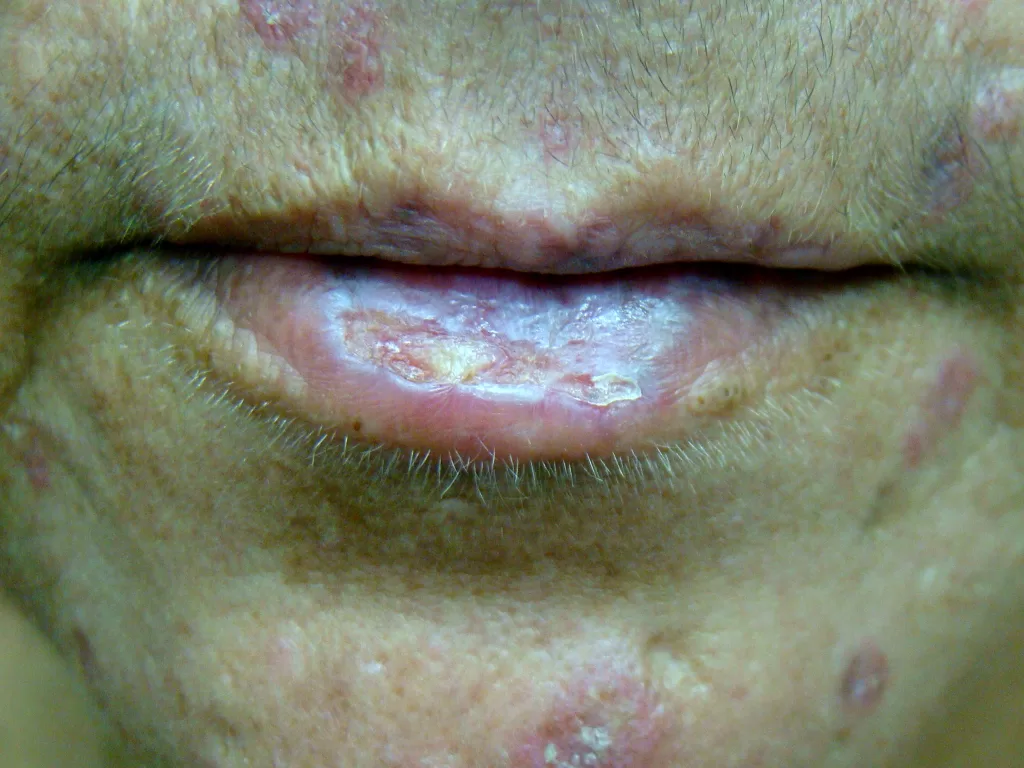
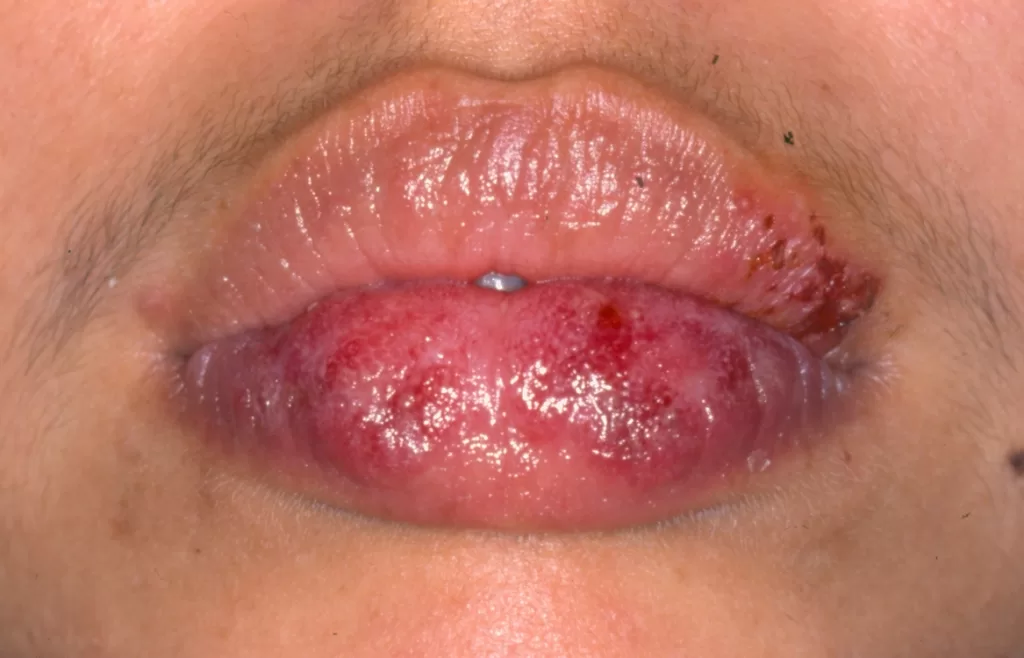
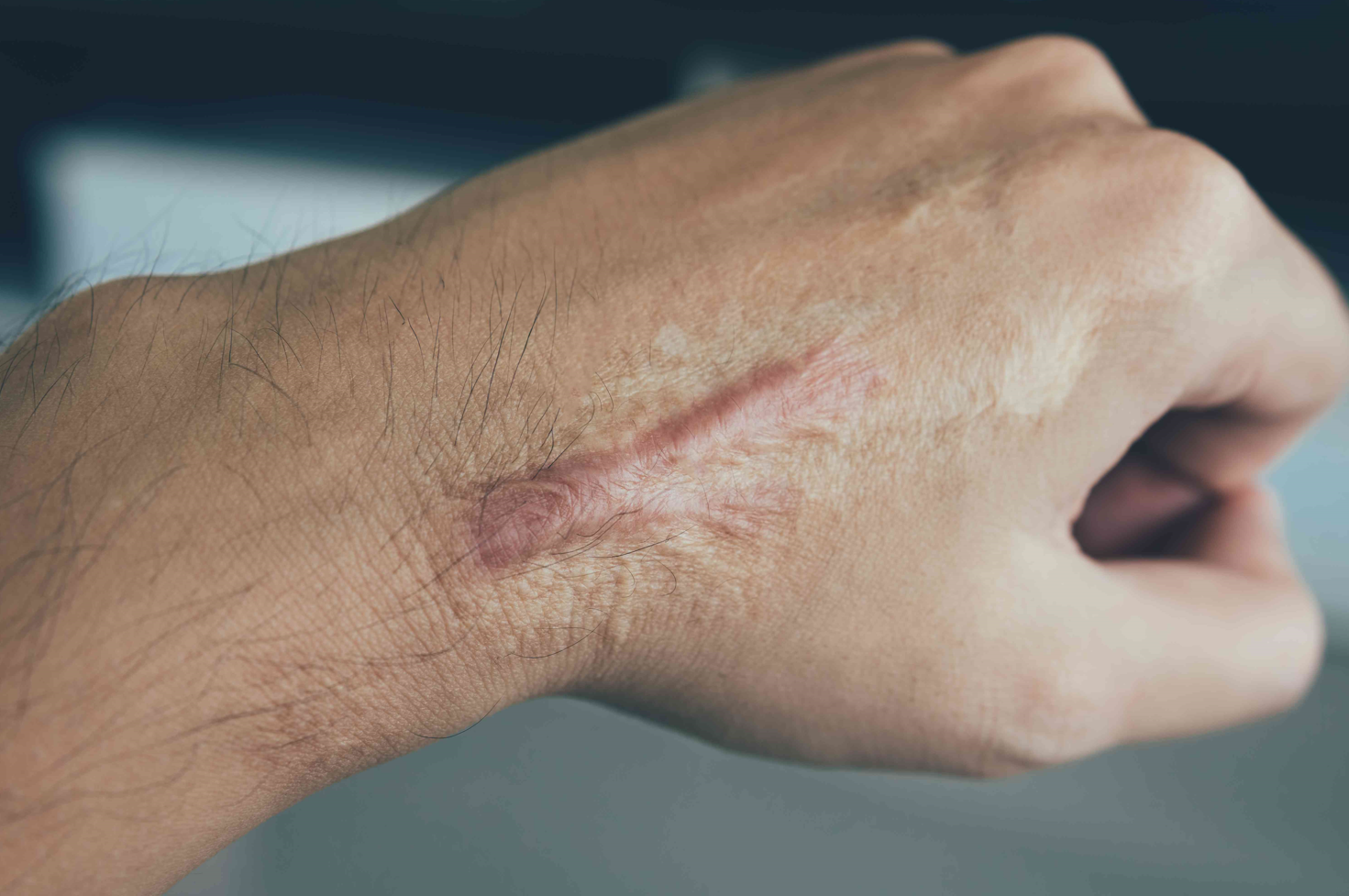
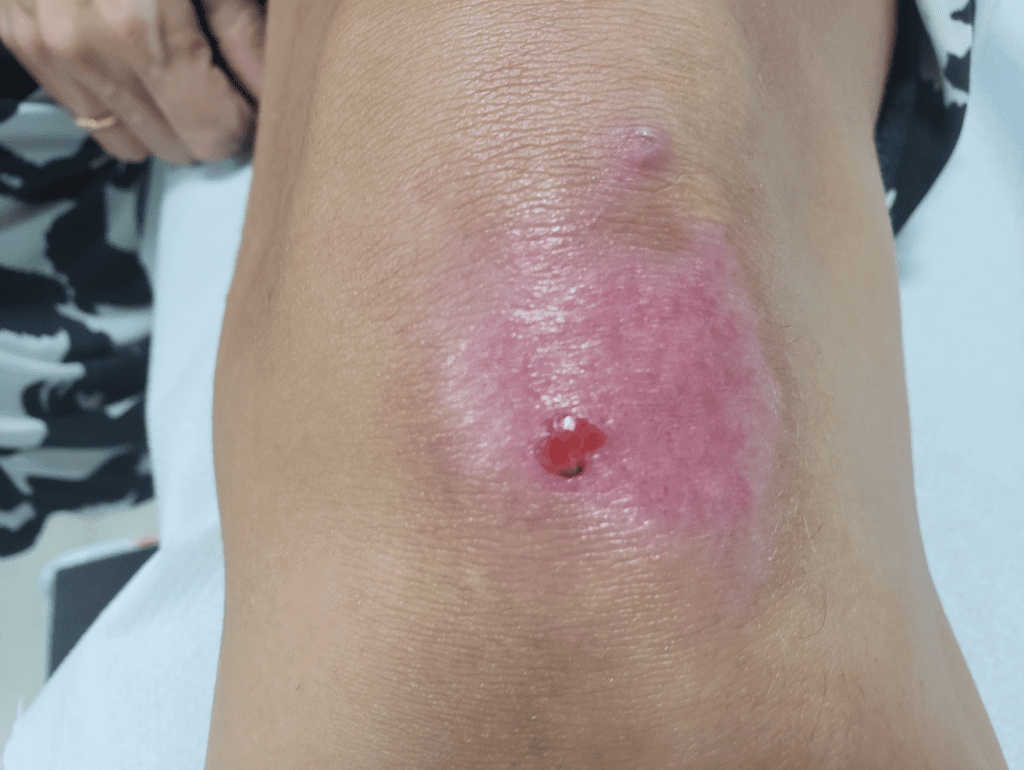
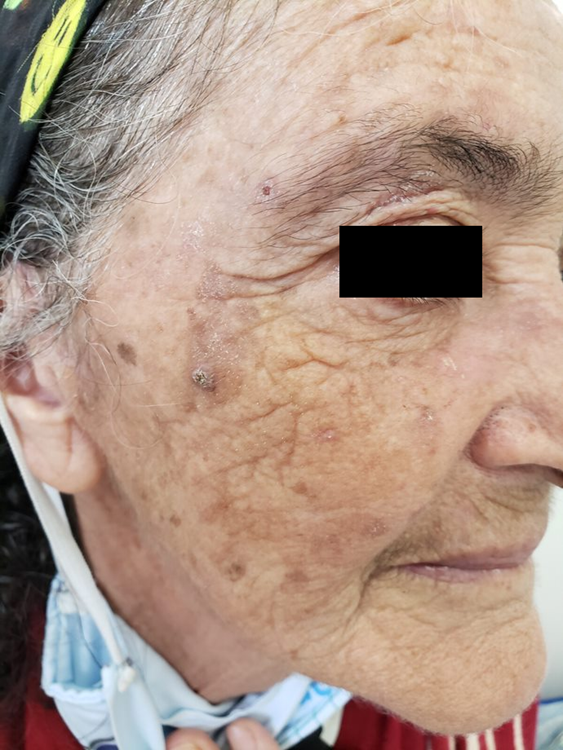
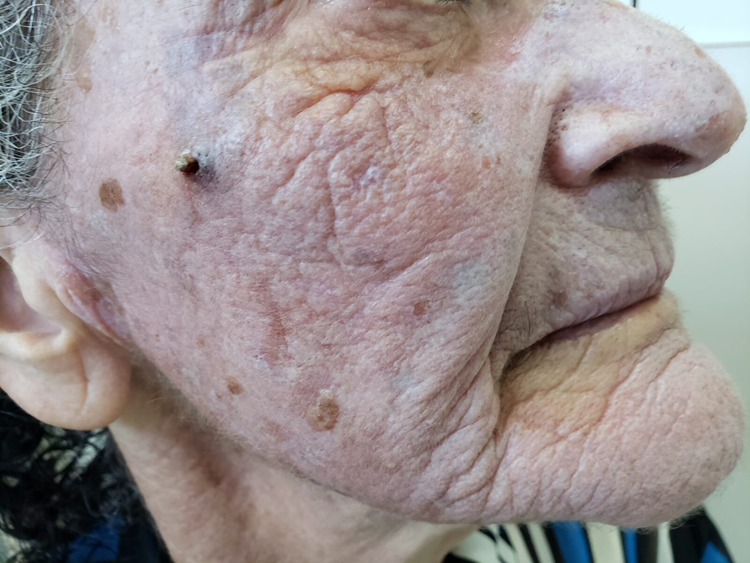
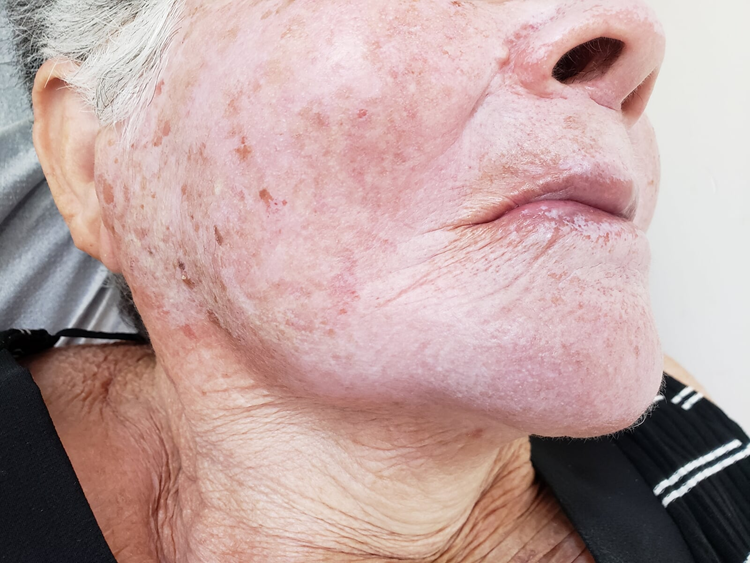
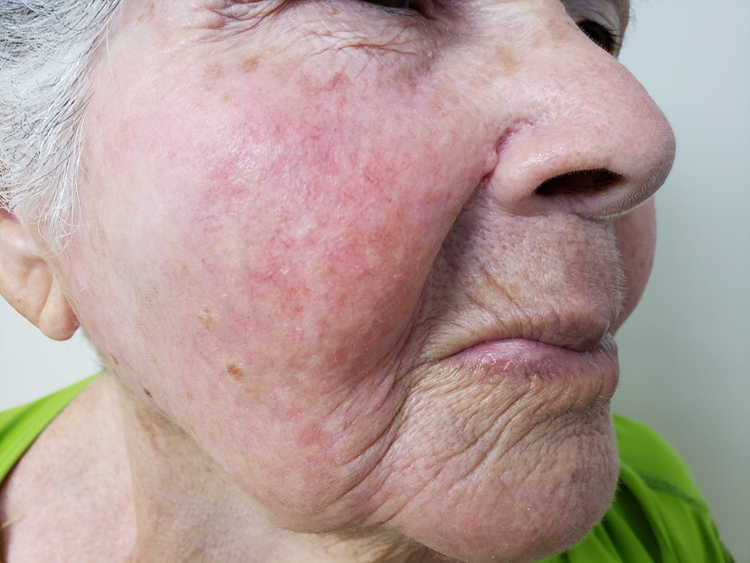
- Textura: Firme ao toque e indolor, o que pode levar a ser frequentemente negligenciada. (fotos 1 e 2))
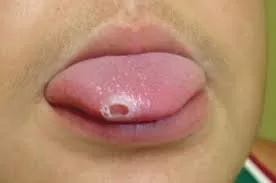
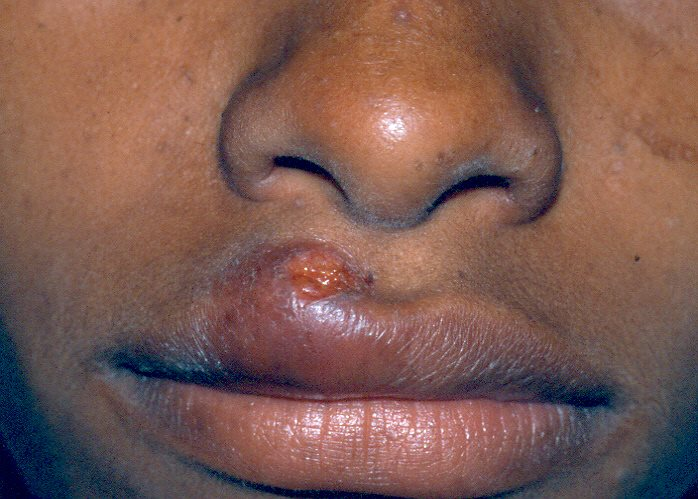
Localização Comum do Cancro:
- Homens: Principalmente na glande (pênis), sulco balanoprepucial e corpo do pênis.
- Mulheres: Grandes e pequenos lábios, clitóris e colo uterino.
- Outras Áreas: Anus e reto, especialmente em indivíduos que têm relações sexuais anais.
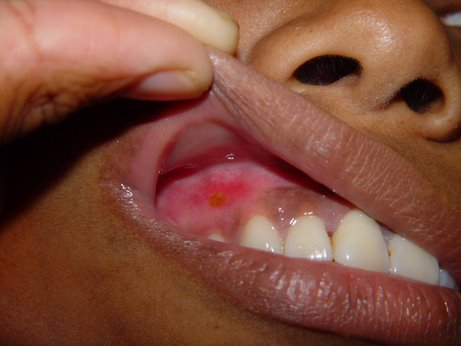
Na boca, resultante de relações orogenitais, mais frequente no lábio, se manifesta como feridas recobertas por crostas ou inflamação e compromete até as amígdalas. (Foto 2)
Duração e Evolução
O cancro sifilítico desaparece naturalmente, após cerca de 4 semanas, mesmo sem tratamento, e não deixa cicatriz.
No entanto, em casos raros, pode ocorrer uma combinação de infecções, conhecida como cancro misto de Rollet, quando combina características de cancro mole e duro.
Linfonodos Afetados
Como resposta imunológica, os linfonodos ( “inguas”) próximos à localização do cancro (como os da virilha ou abaixo da mandíbula) podem aumentar de tamanho. Eles são firmes, indolores e não apresentam inflamação.
Sífilis Secundária: Sintomas e Características
A sífilis secundária surge como uma reação do sistema imunológico à disseminação da bactéria.
Manifesta-se entre 2 a 6 meses após a infecção e, em muitos casos, ocorre 6 a 8 semanas após o aparecimento do cancro. Notavelmente, o cancro pode ainda estar presente nesta fase, especialmente em portadores de AIDS.
Por que tratar na fase secundária?
Embora as lesões desta fase desapareçam mesmo sem tratamento, é crucial tratá-las para evitar complicações graves que surgem nas fases posteriores.
Manifestações da Sífilis Secundária:
- Febre
- Cefaleia (dor de cabeça)
- Mal-estar
- Anorexia (falta de apetite)
- Dor de garganta
- Mialgia (dor muscular)
- Artralgia (dor nas articulações)
- Lacrimejamento
- Perda de peso
Manifestações Cutâneas: As mais comuns, ocorrendo em 80 a 95% dos casos. Incluem:
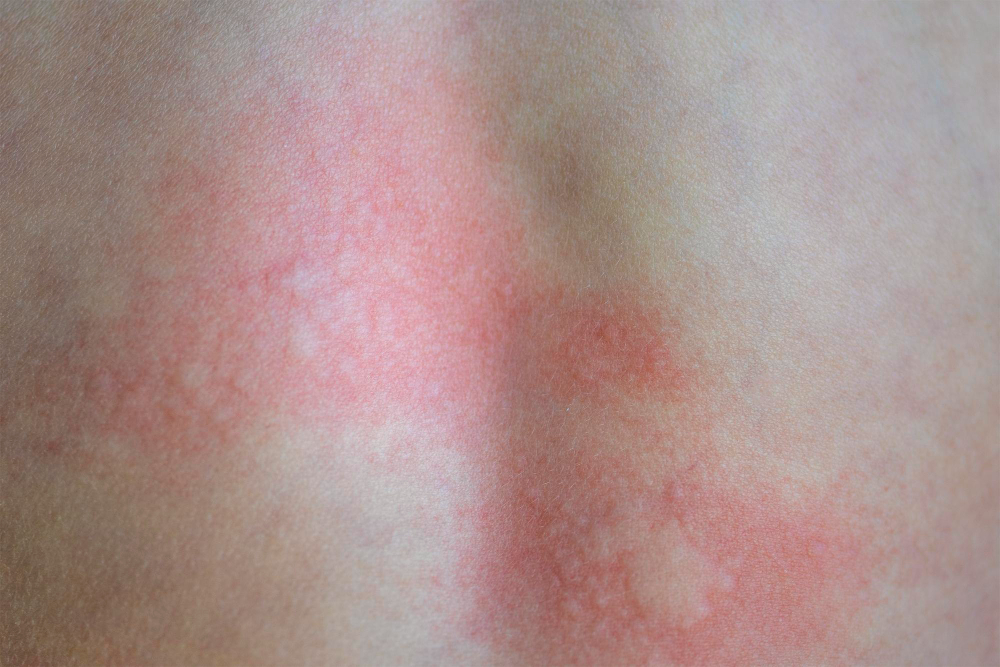
- Roséola sifilítica: Manchas avermelhadas ou de tonalidade cobre.
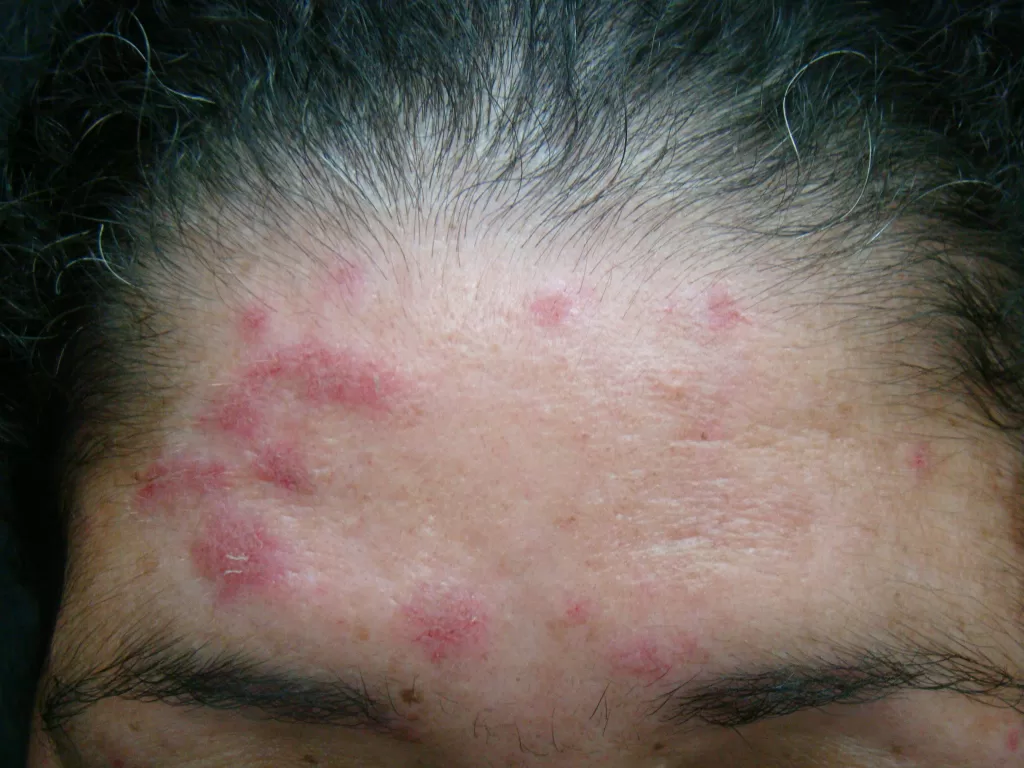
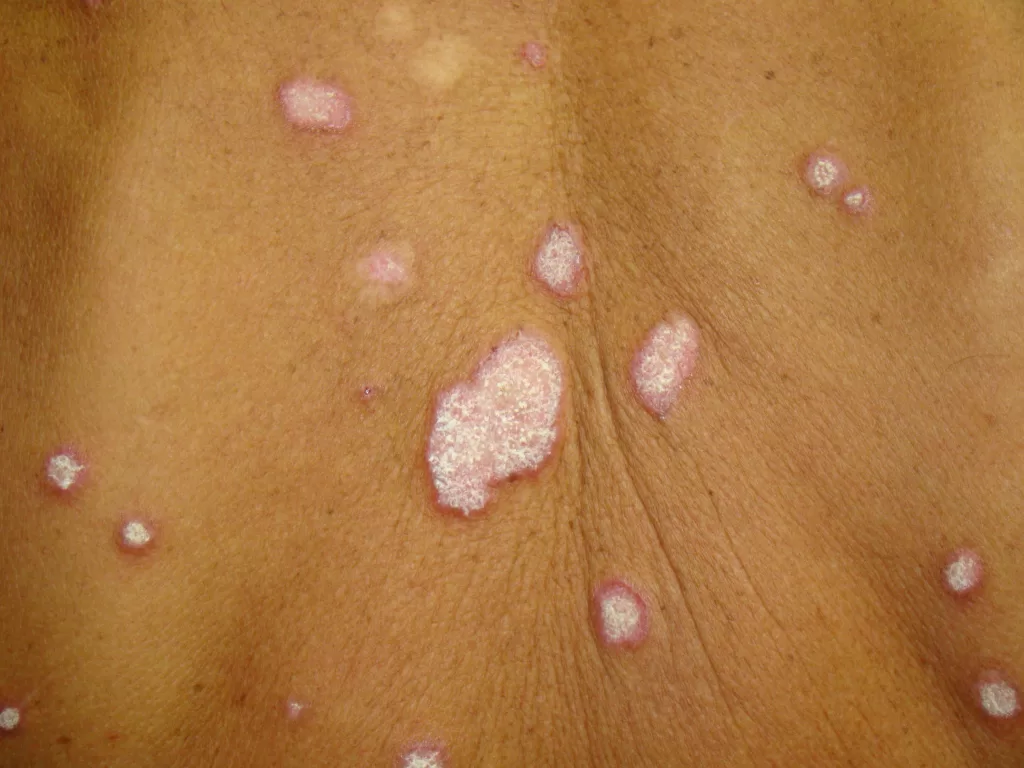
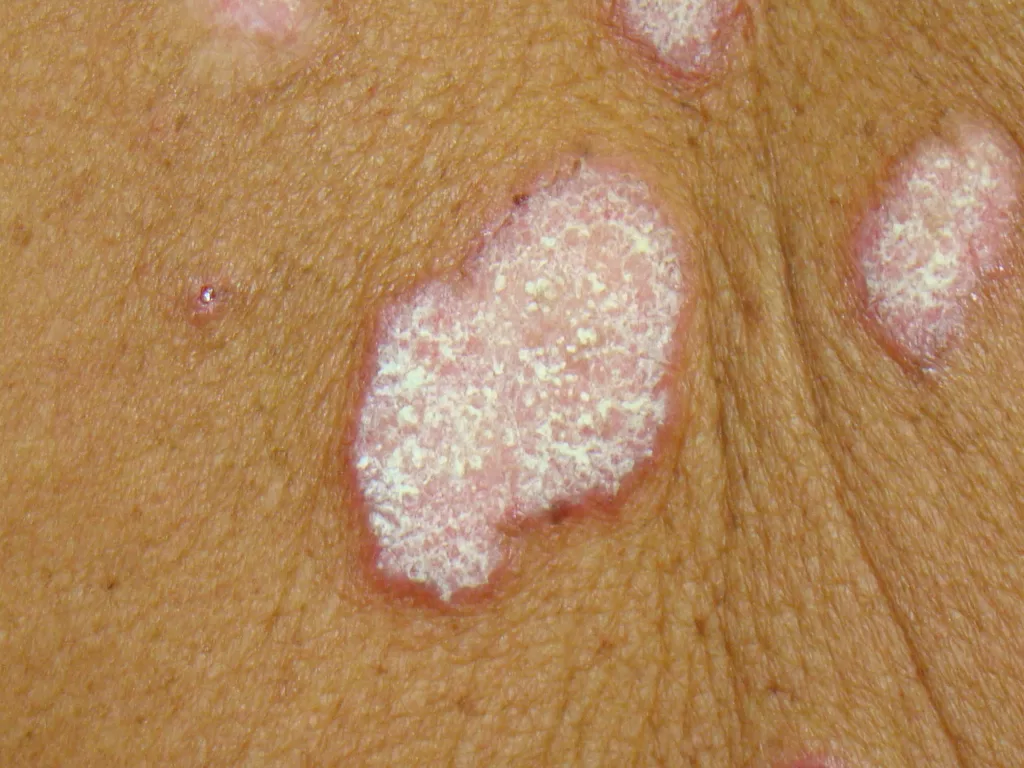
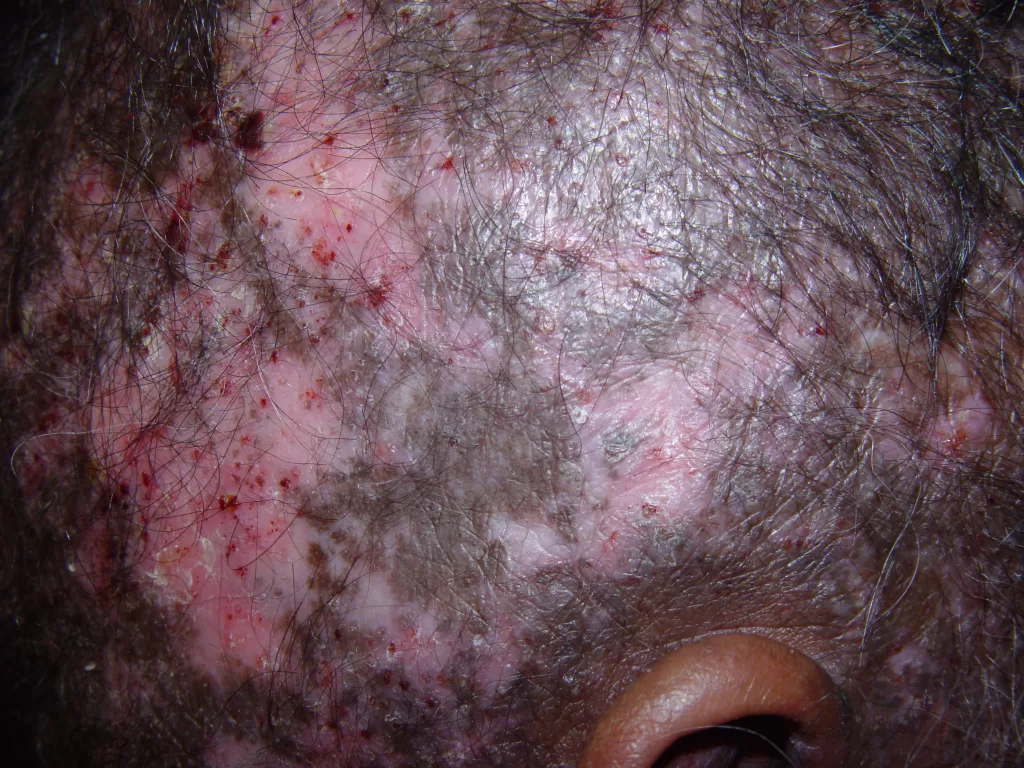
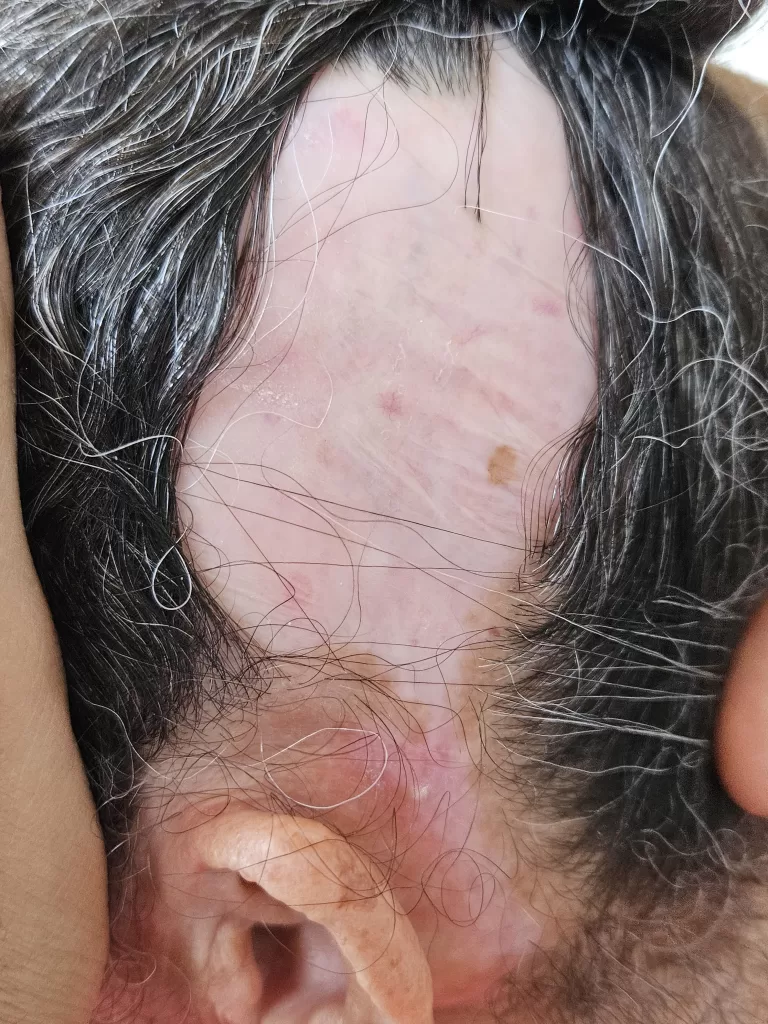
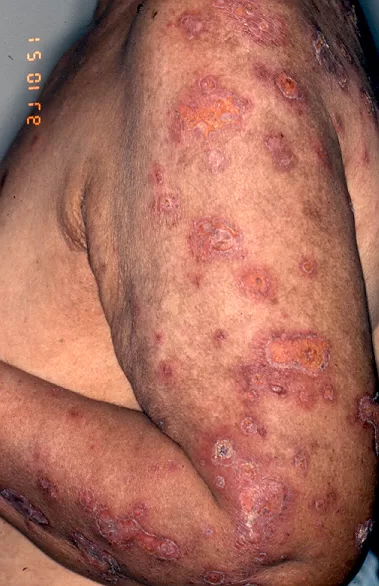
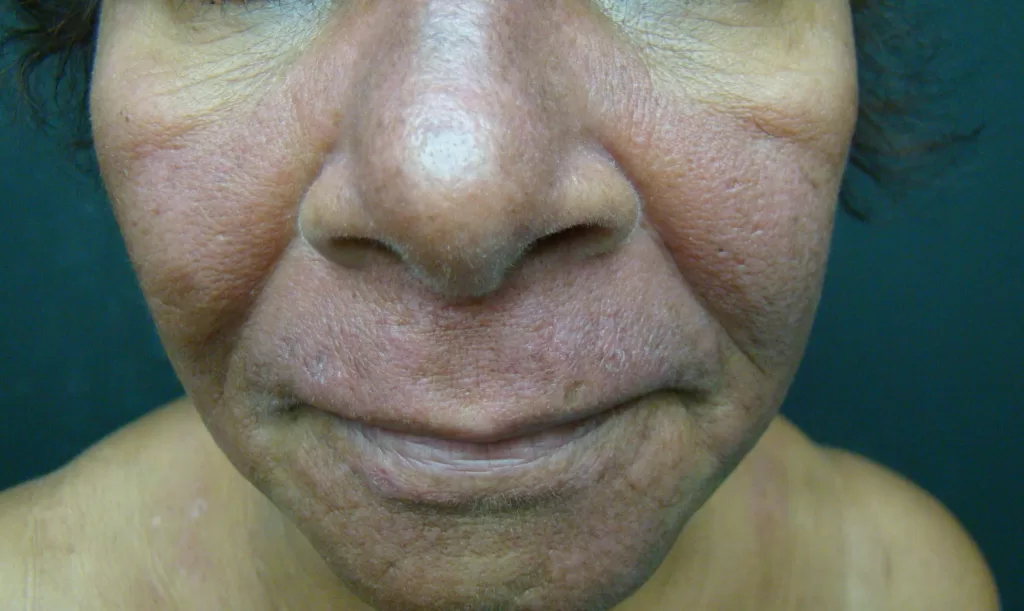
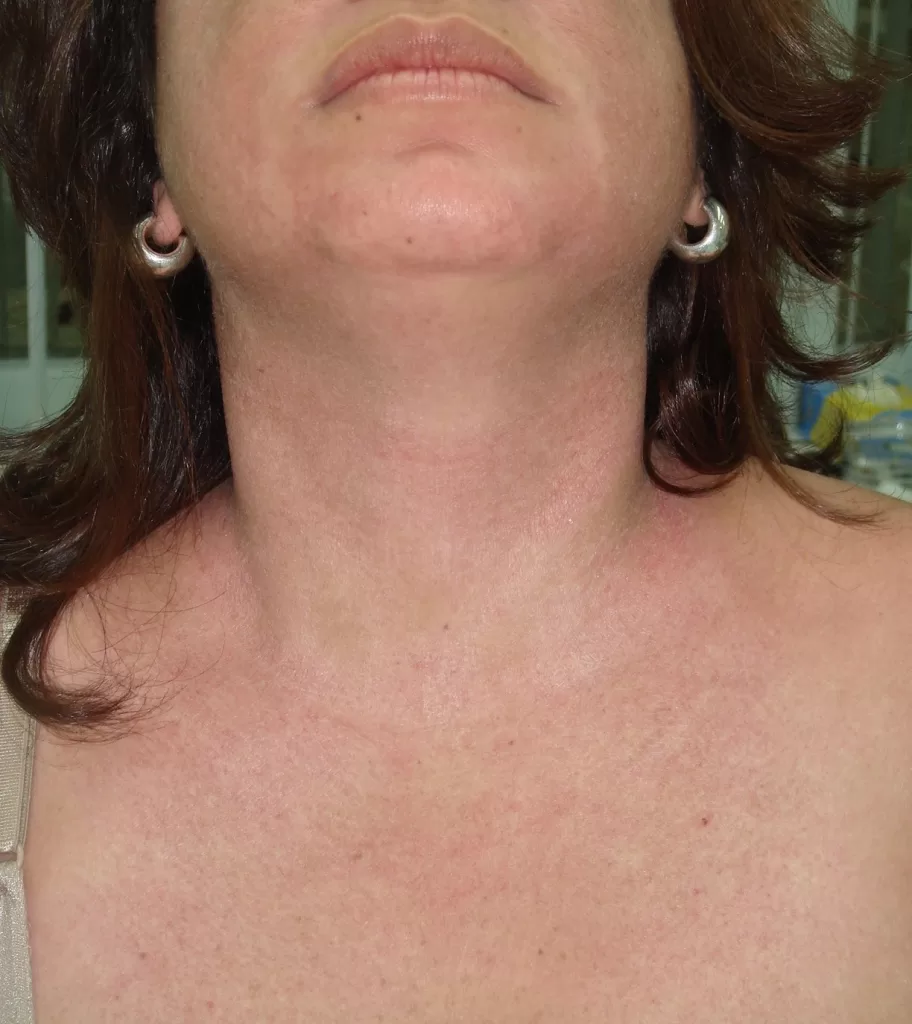
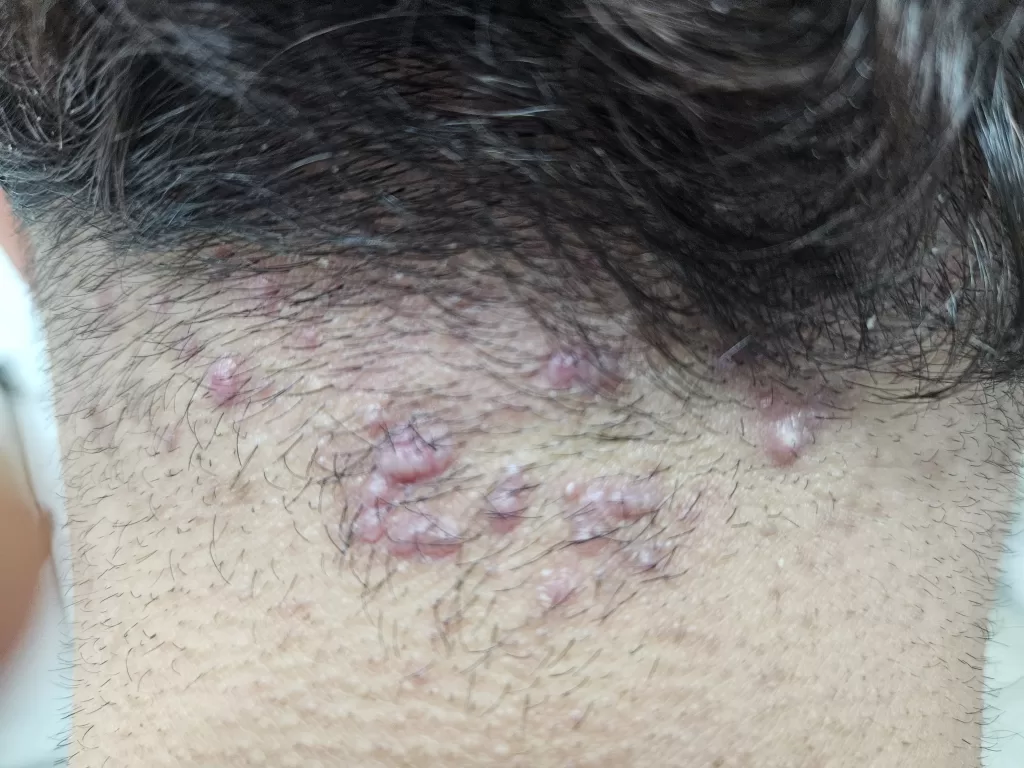
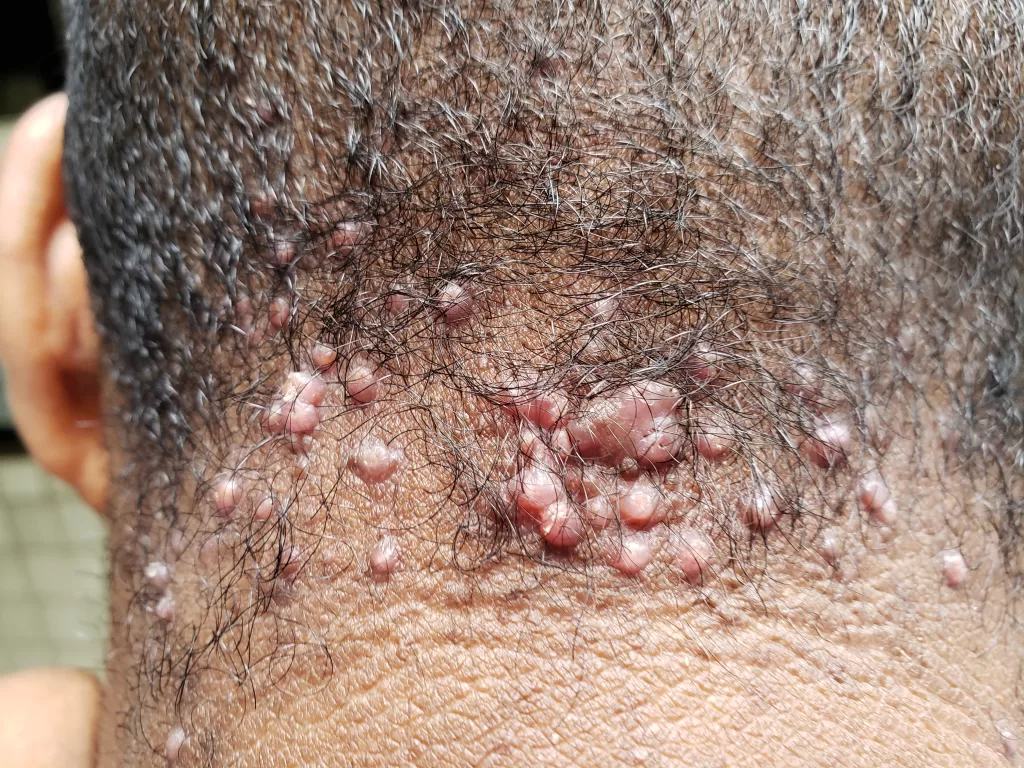
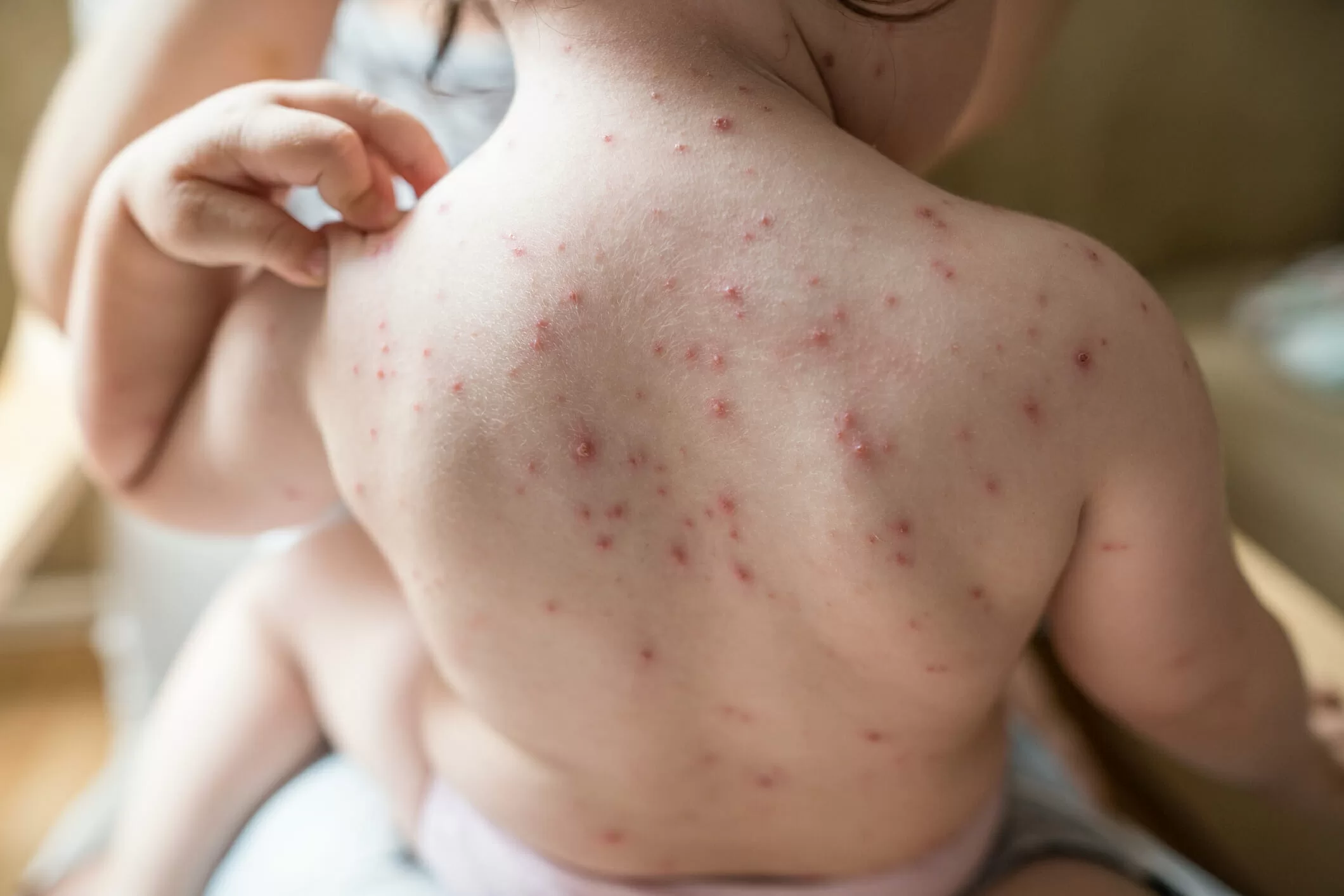
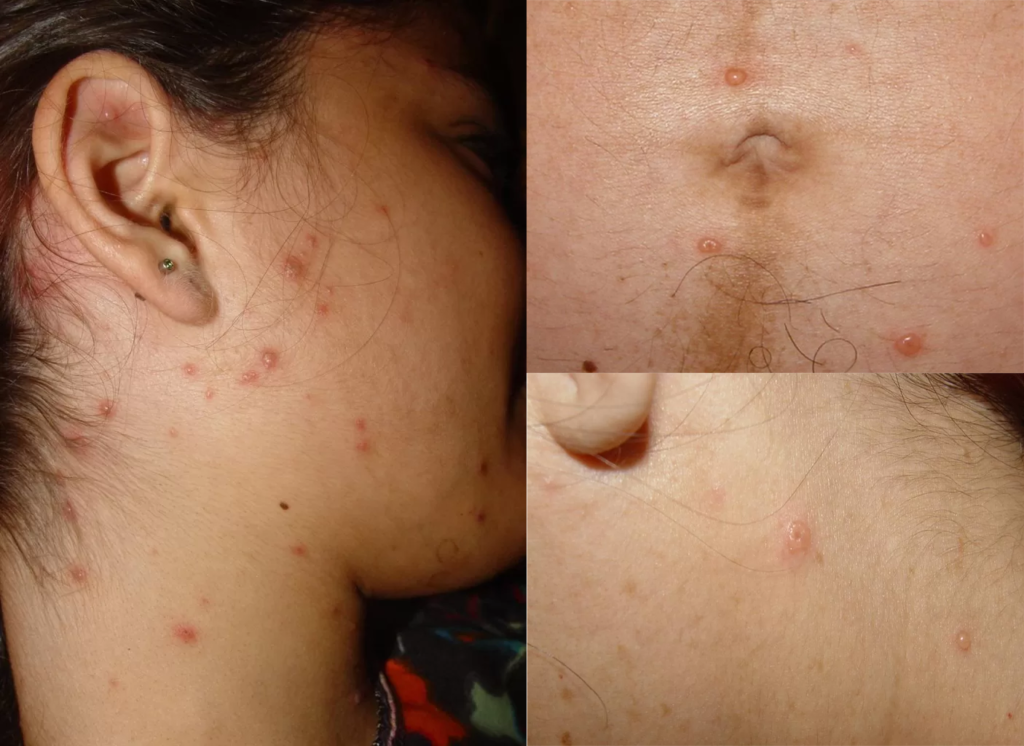
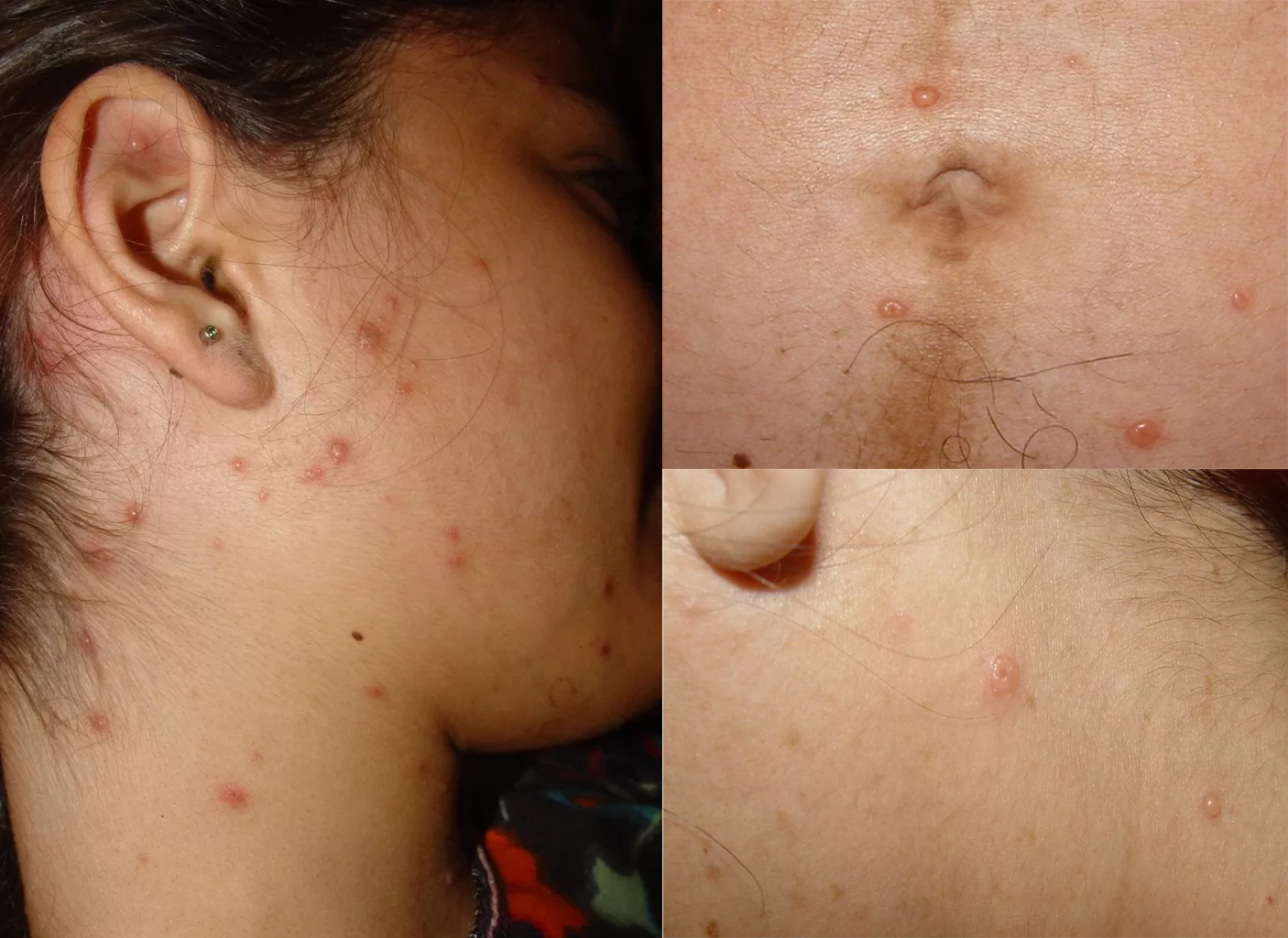
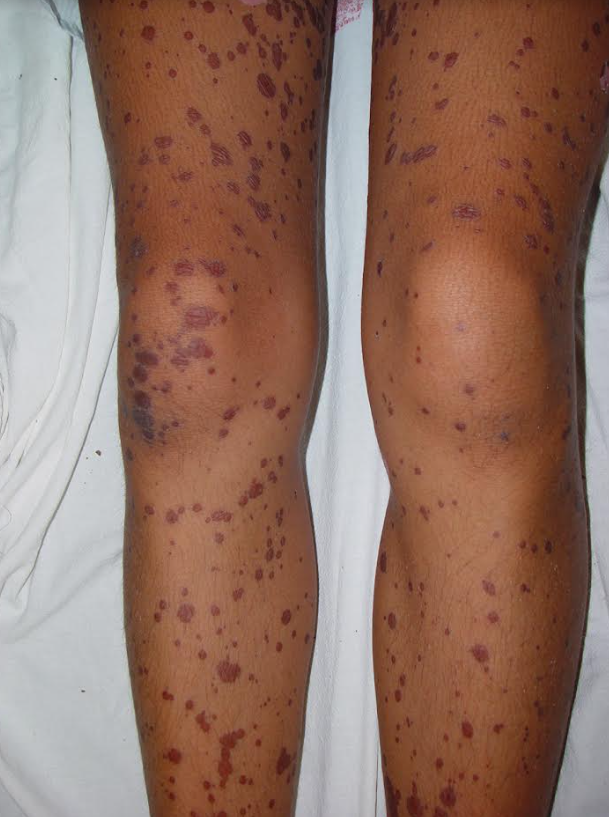
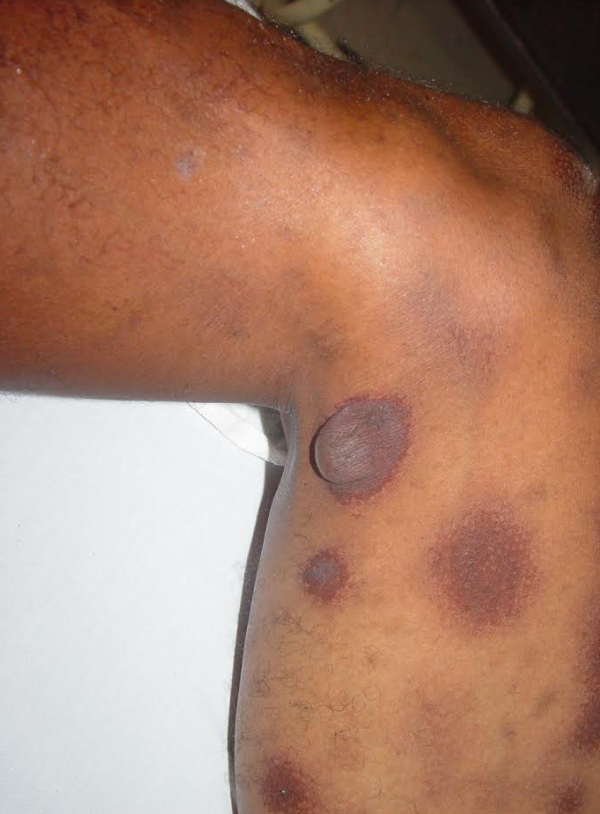
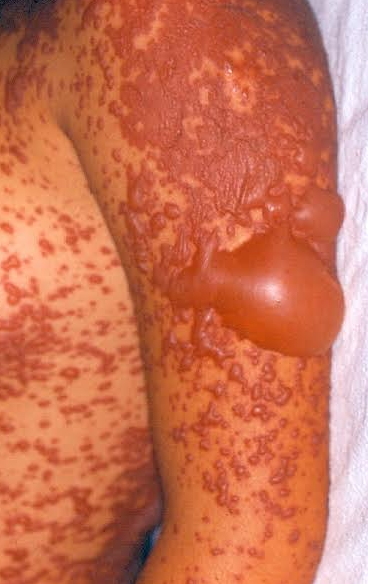
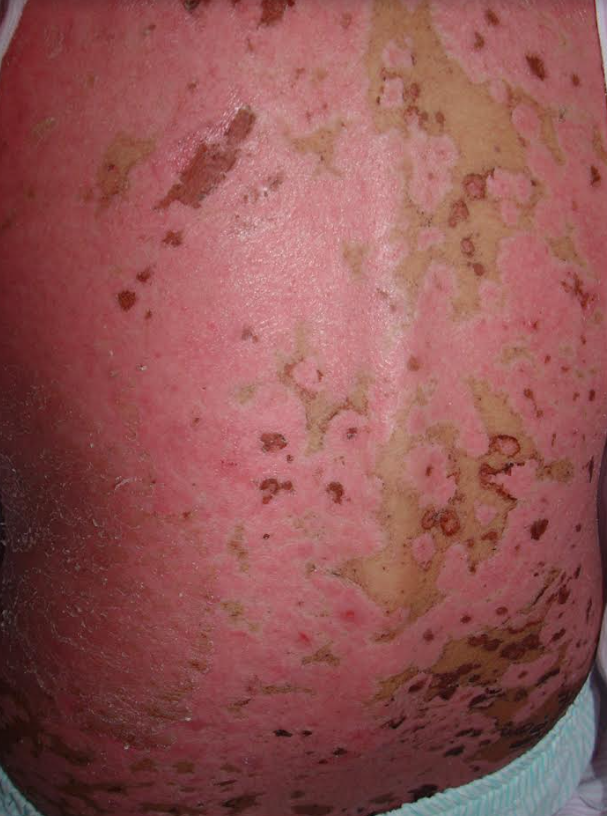
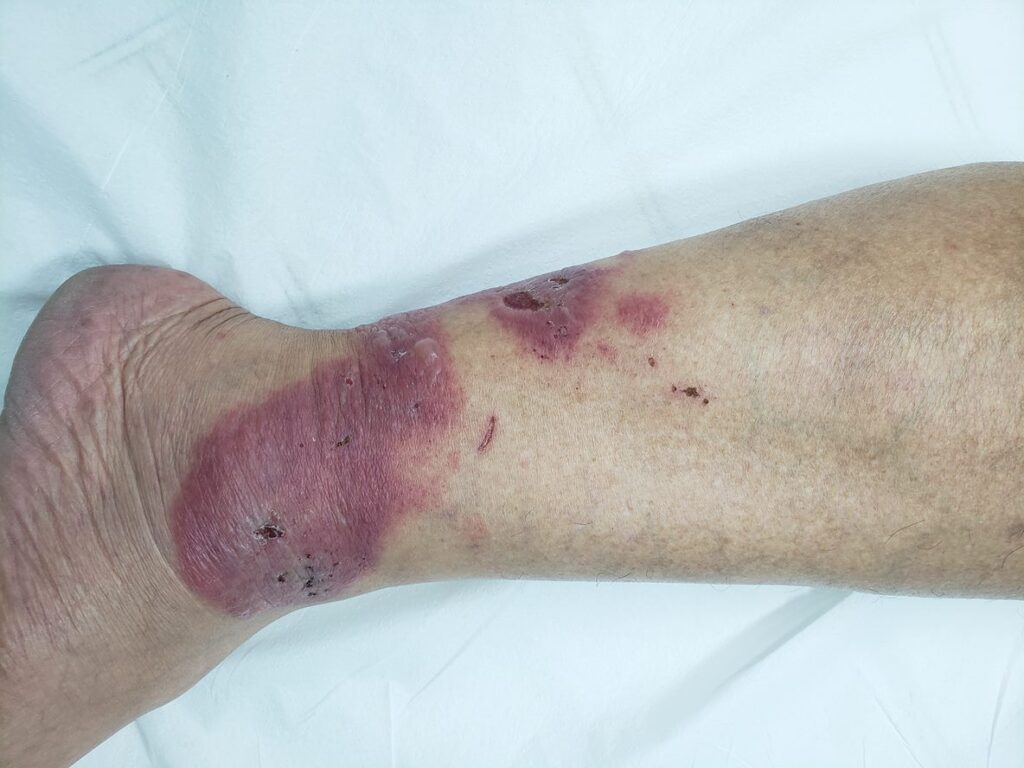
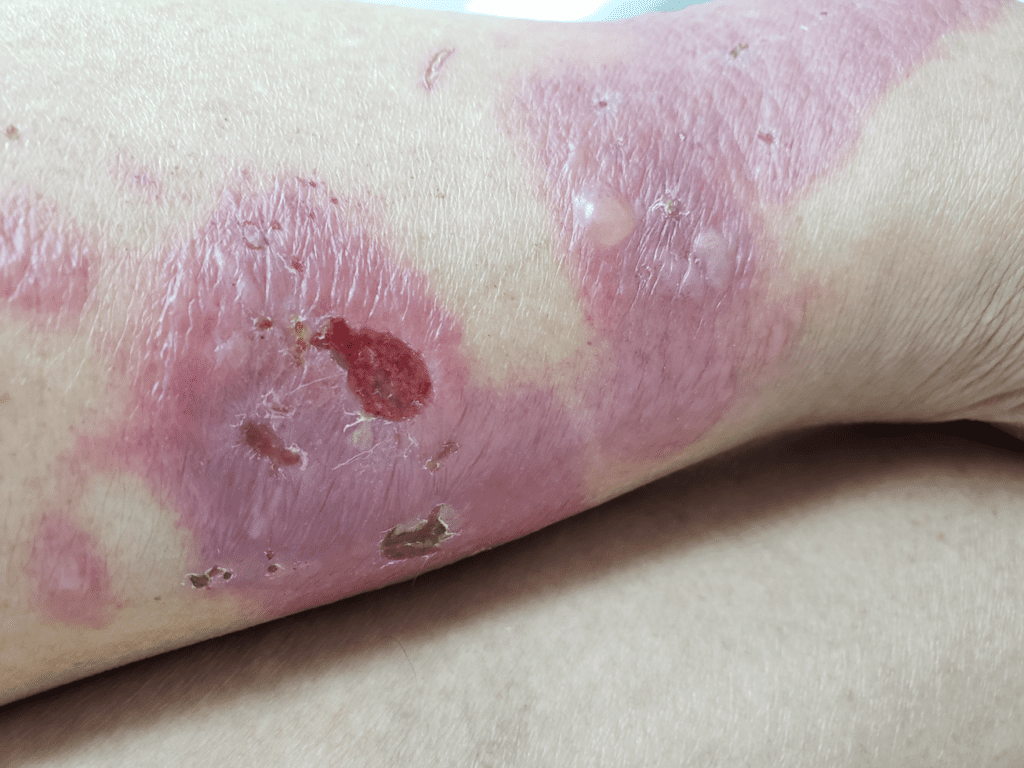
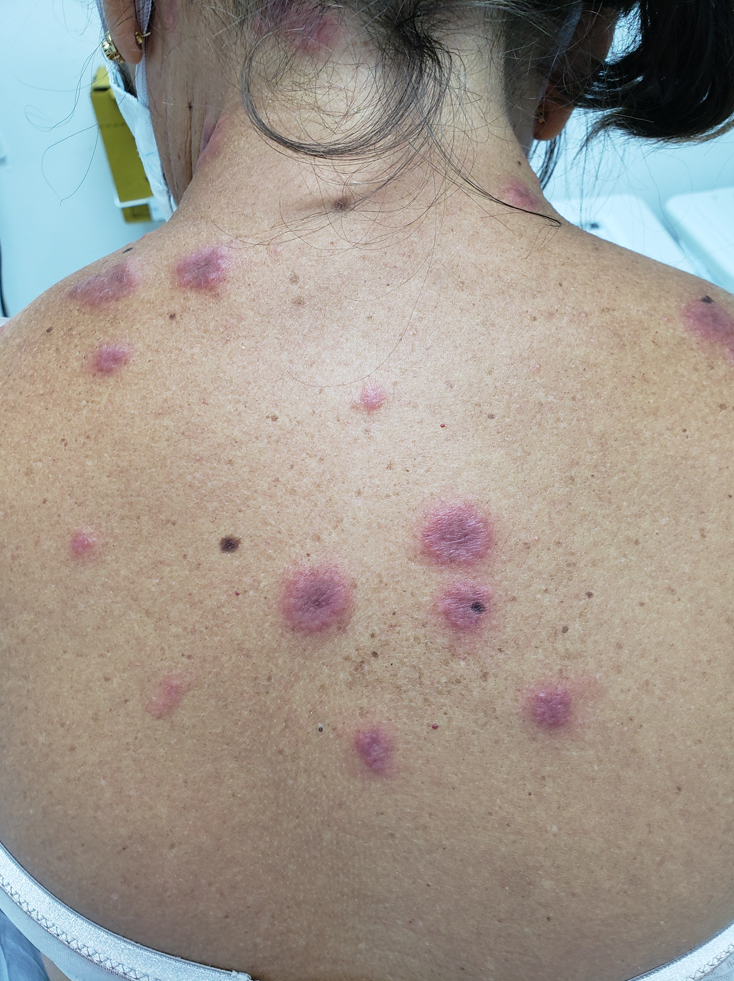
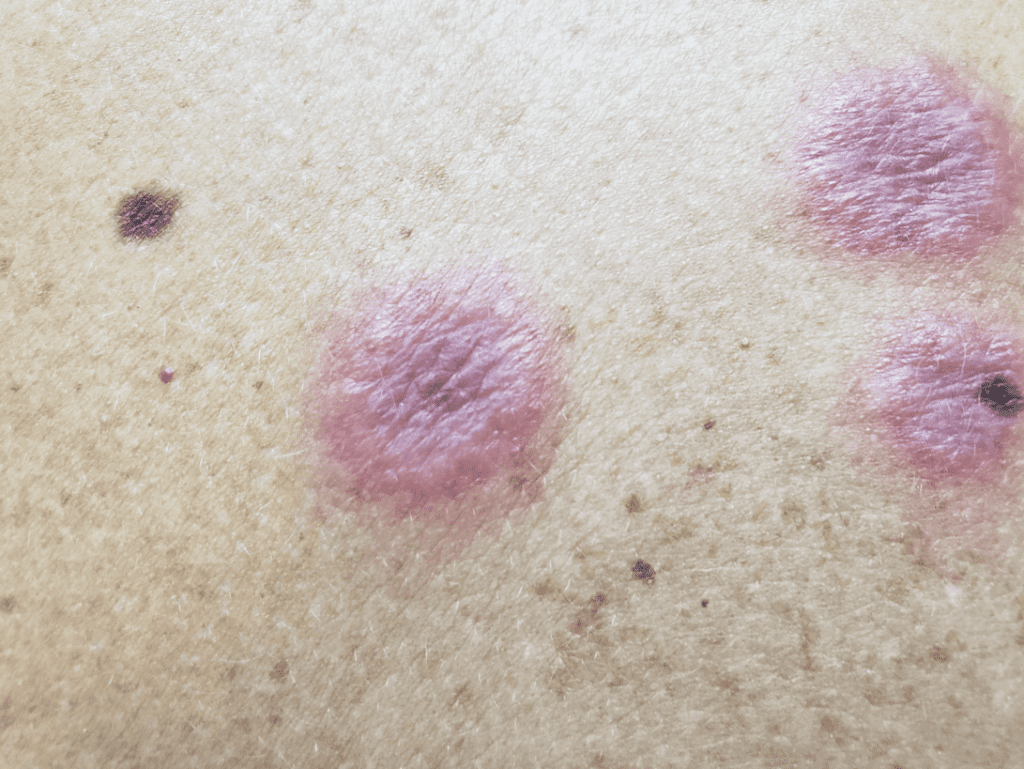
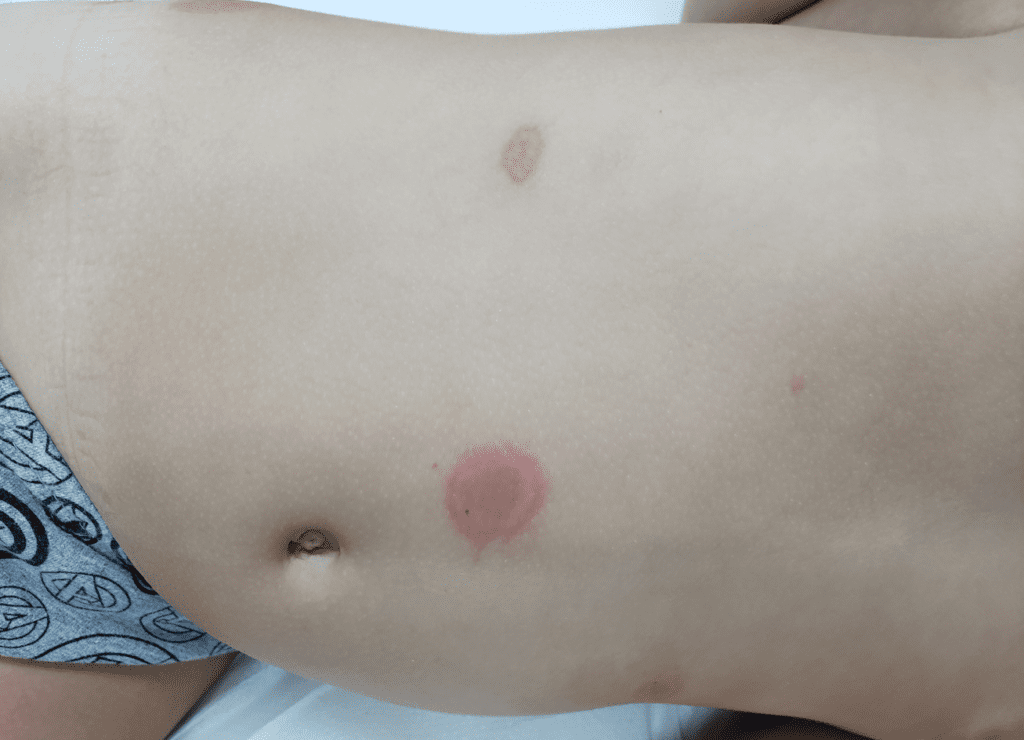
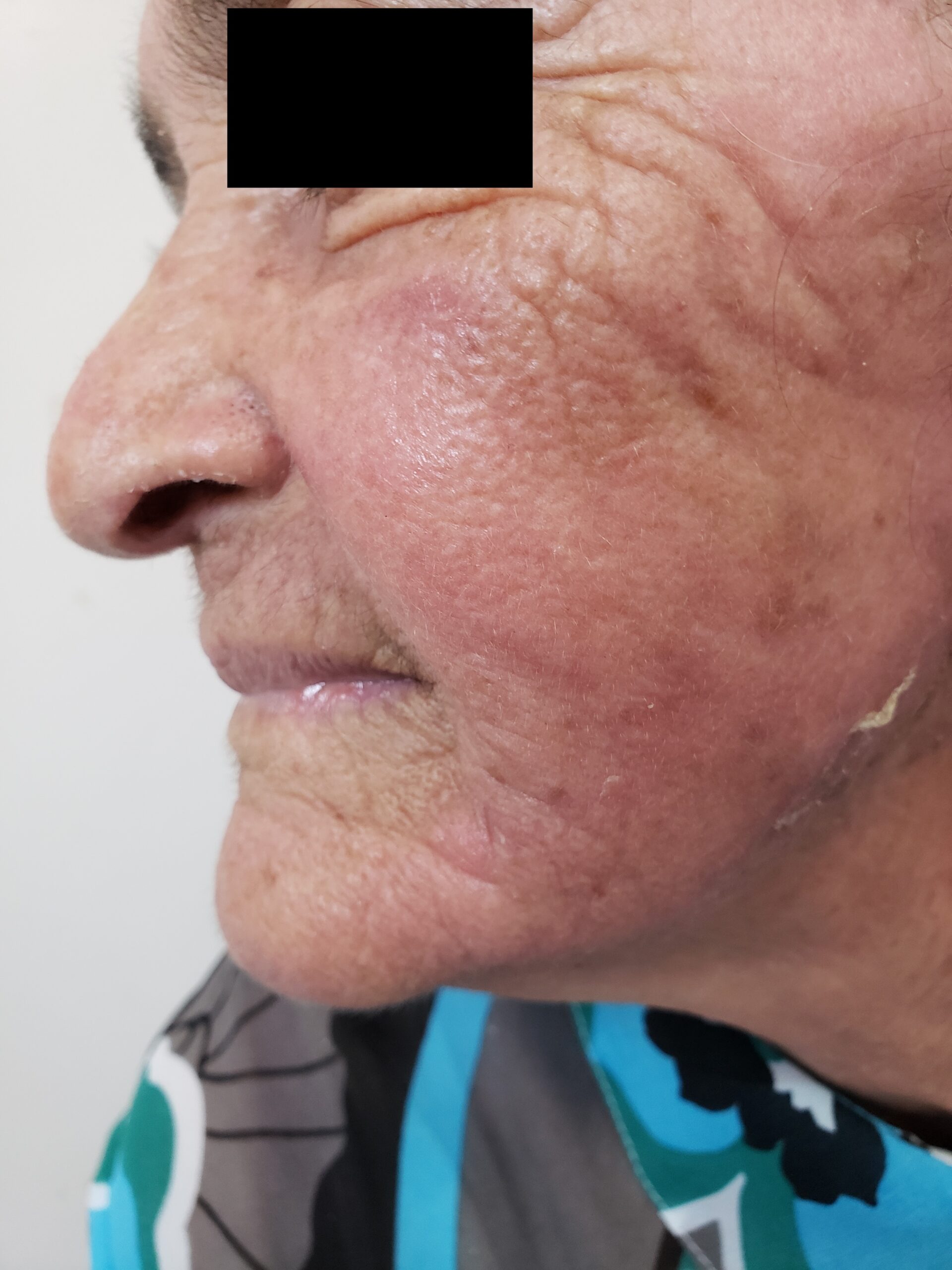
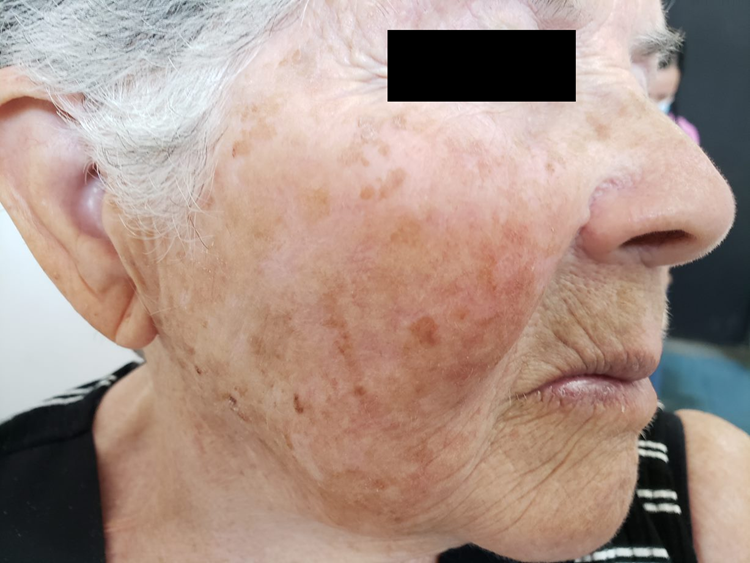
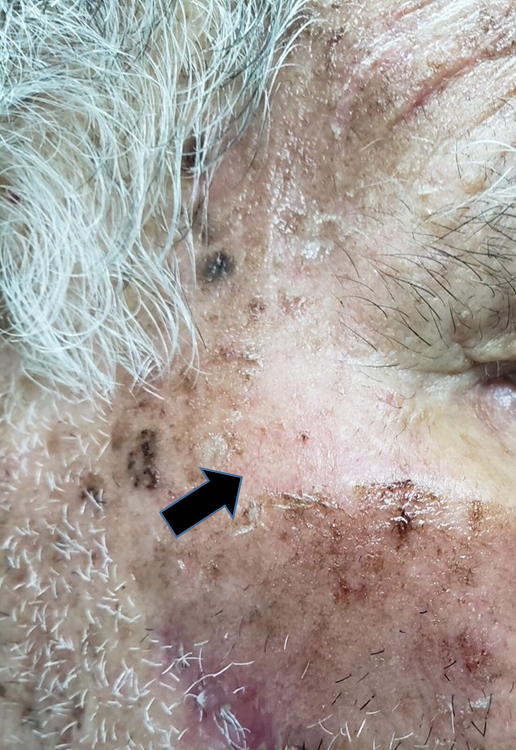
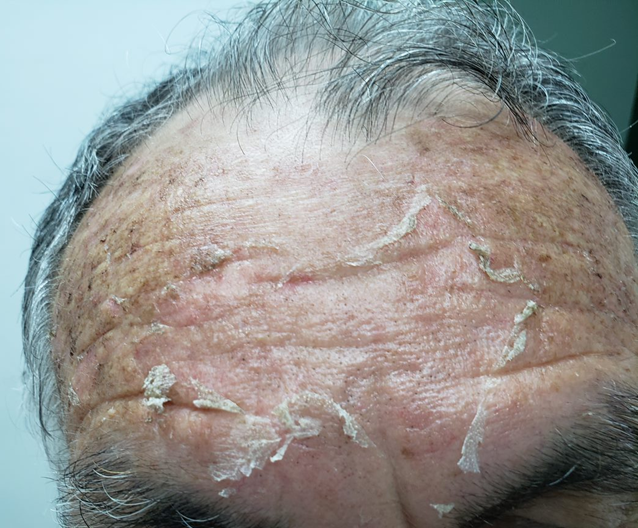
- Sifílide papulosa: Pápulas que surgem com o tempo. (fotos 3 e 4)
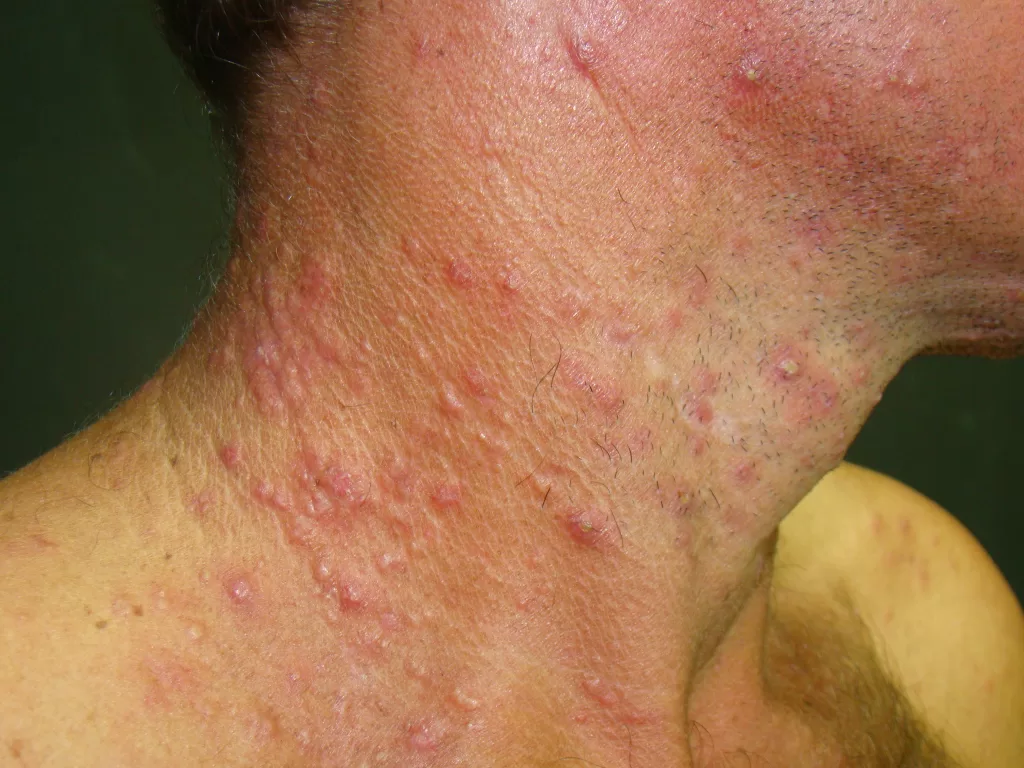
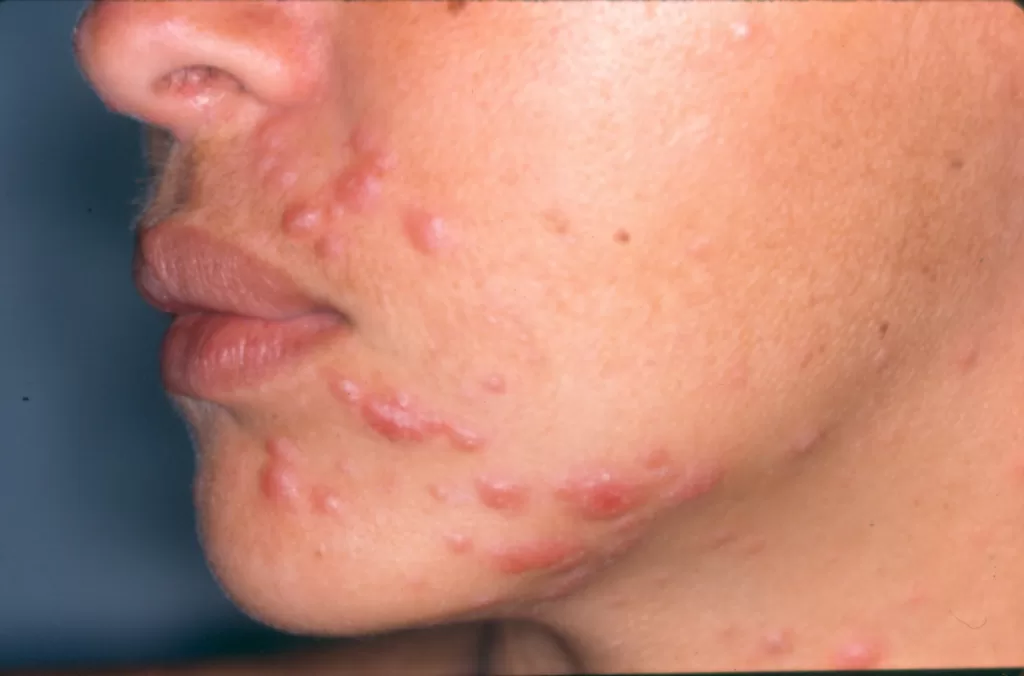
Forma papuloescamosa: Pápulas com escamas (foto 5).
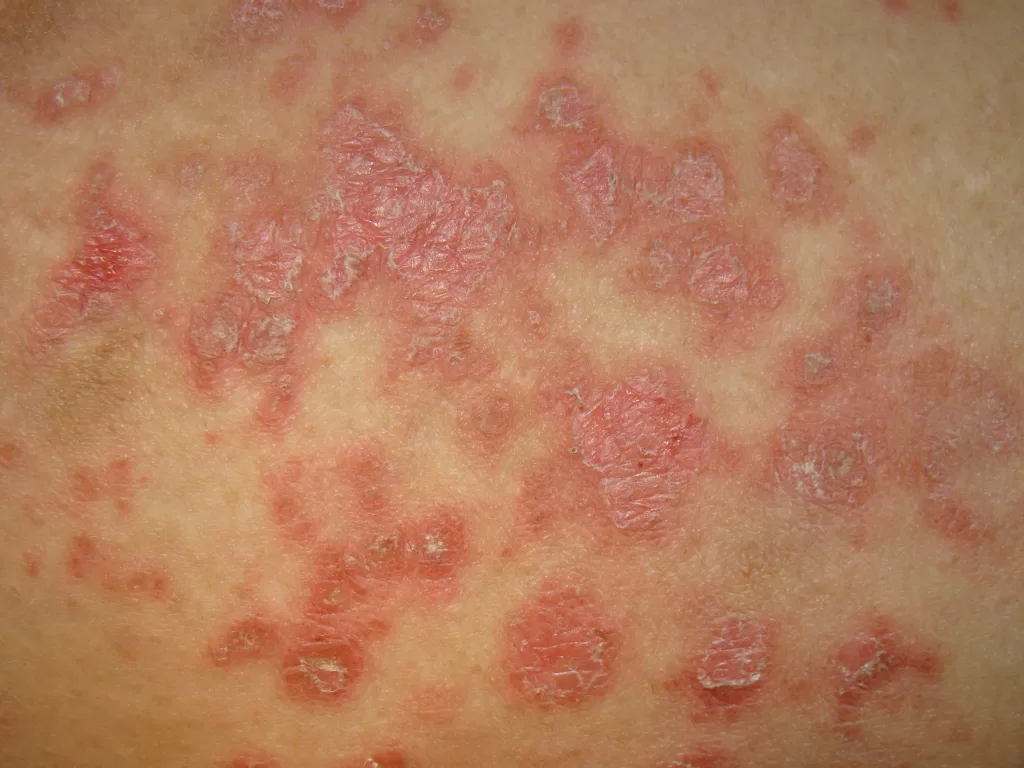
Mescla de manchas e pápulas num mesmo paciente. (Foto 6)
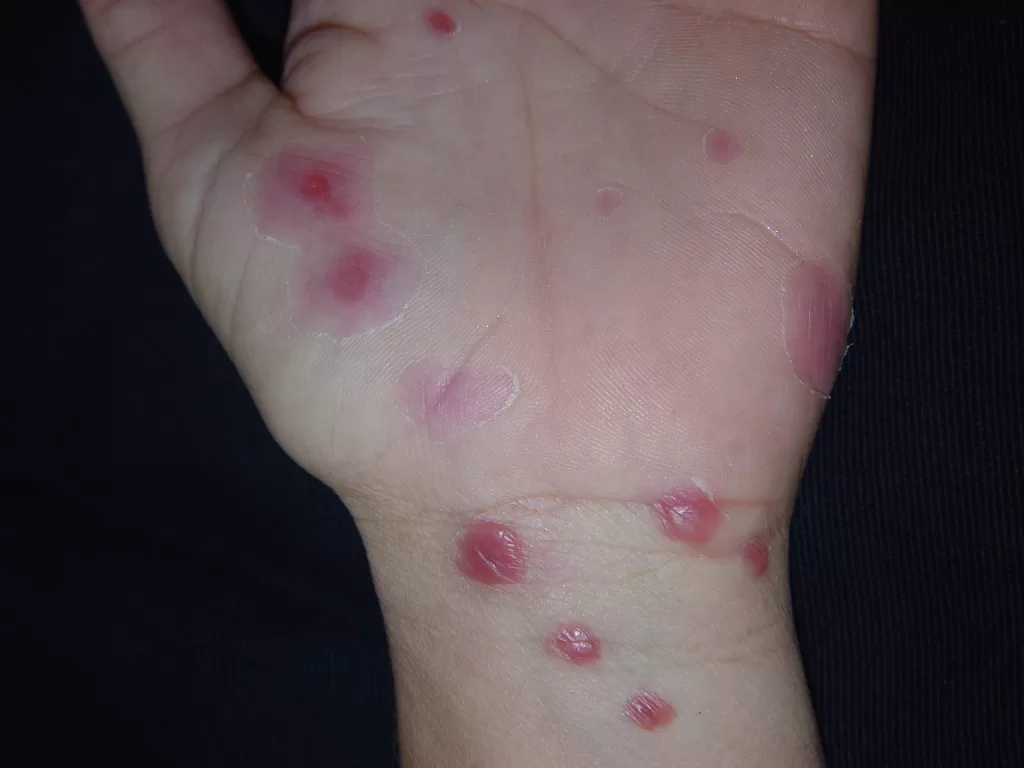
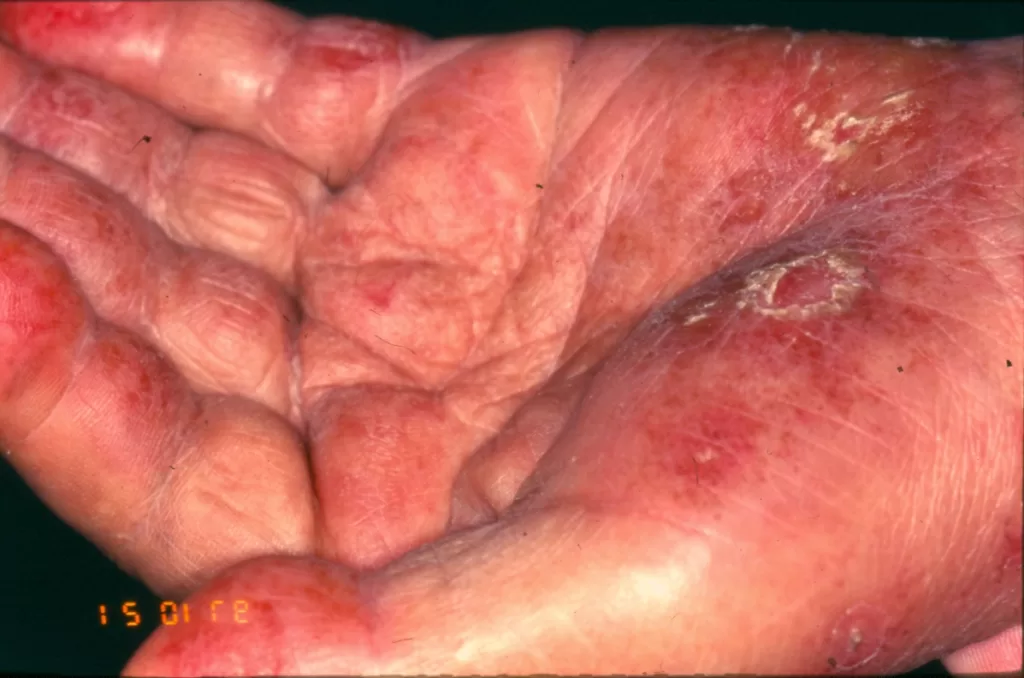
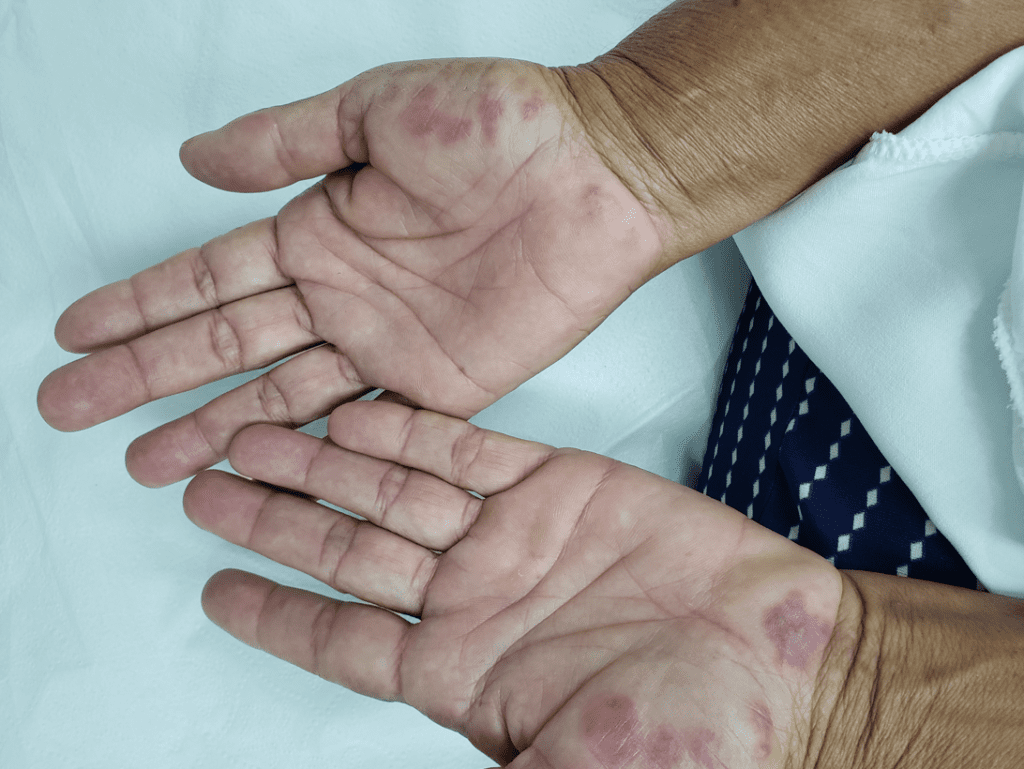
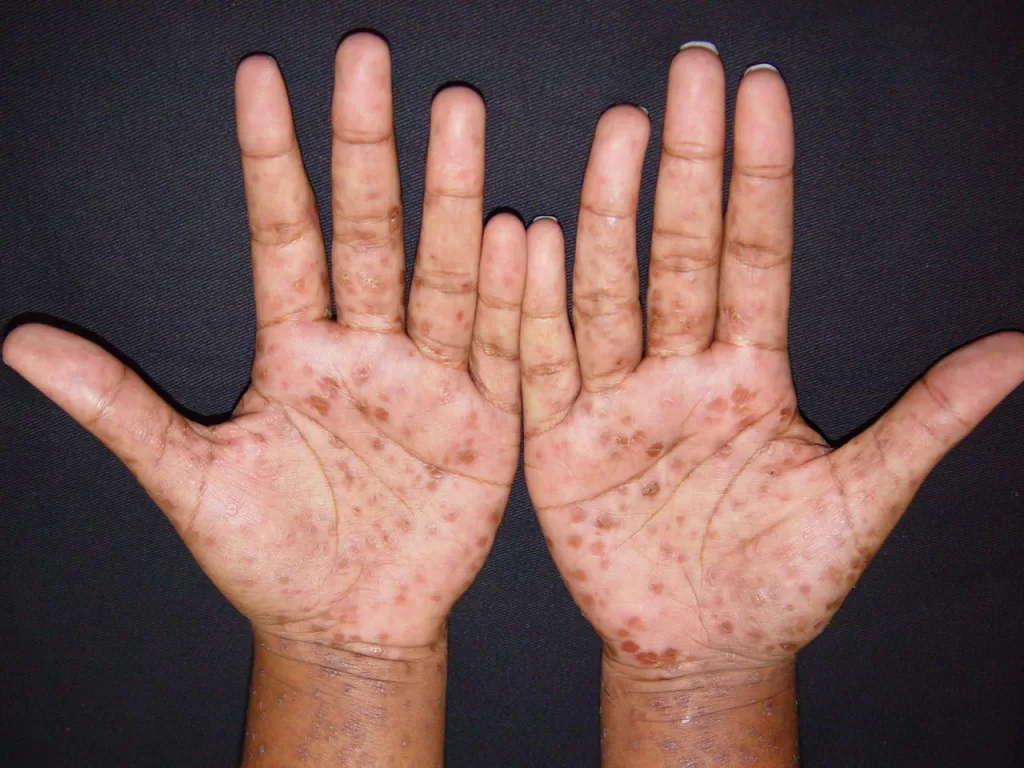
Erupções que reaparecem focadas em áreas como palmas e plantas (fotos 7A e 7B)
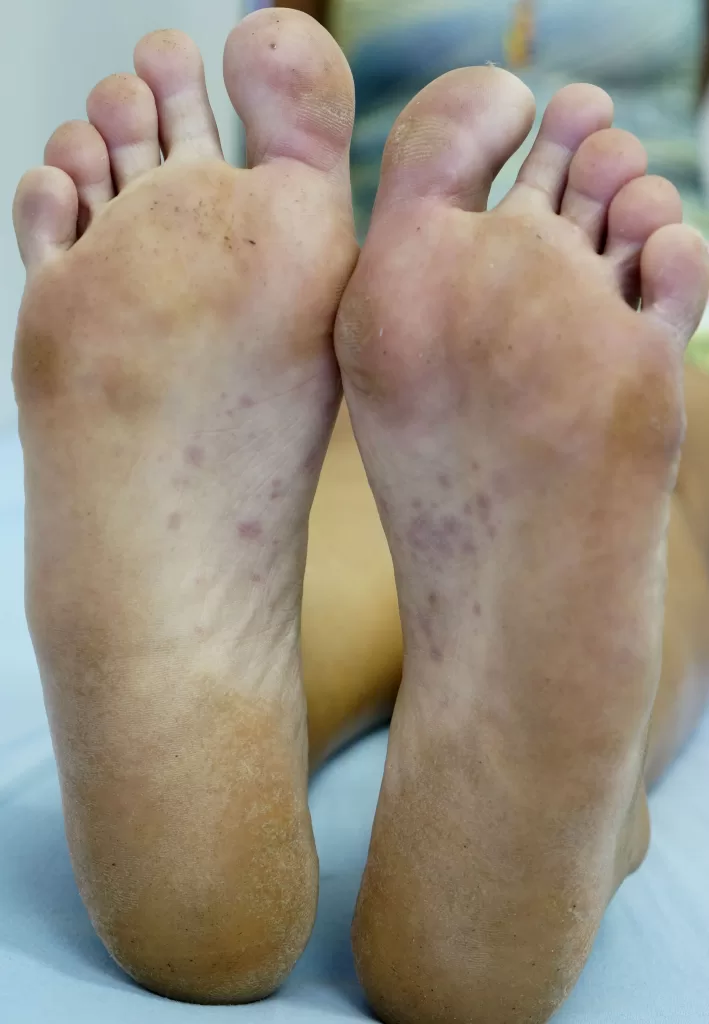
Descamação característica: Conhecida como colar de Biet (fotos 8 e 9)
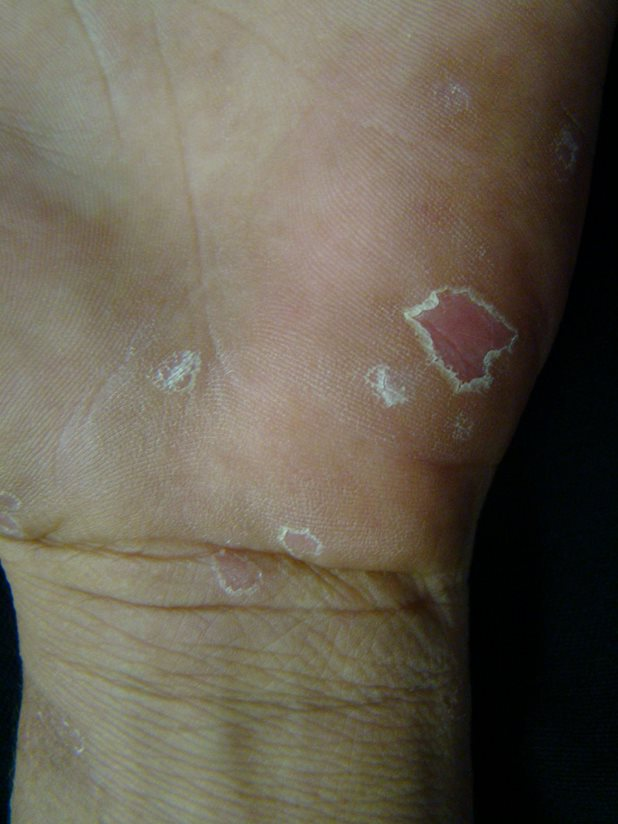
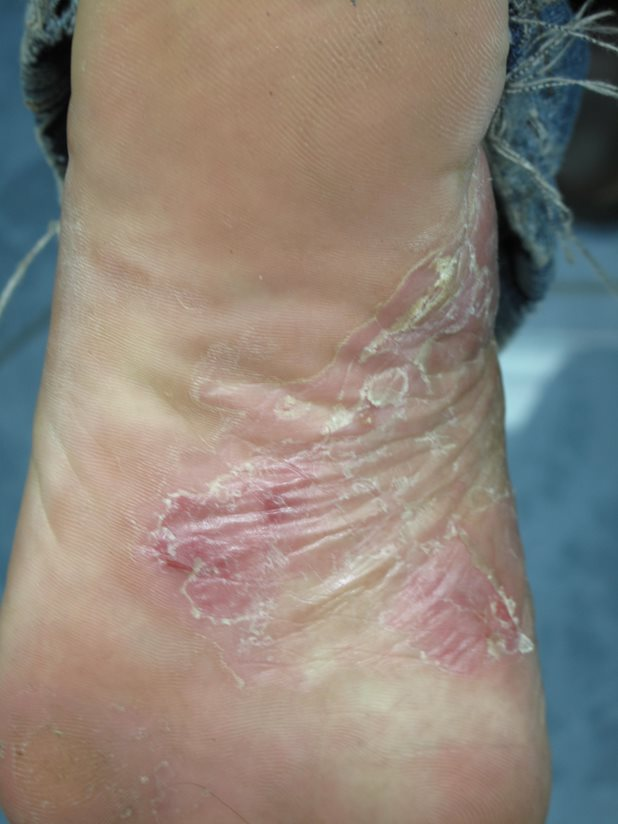
Ulcerações chamadas de condiloma plano, especialmente em áreas de atrito.
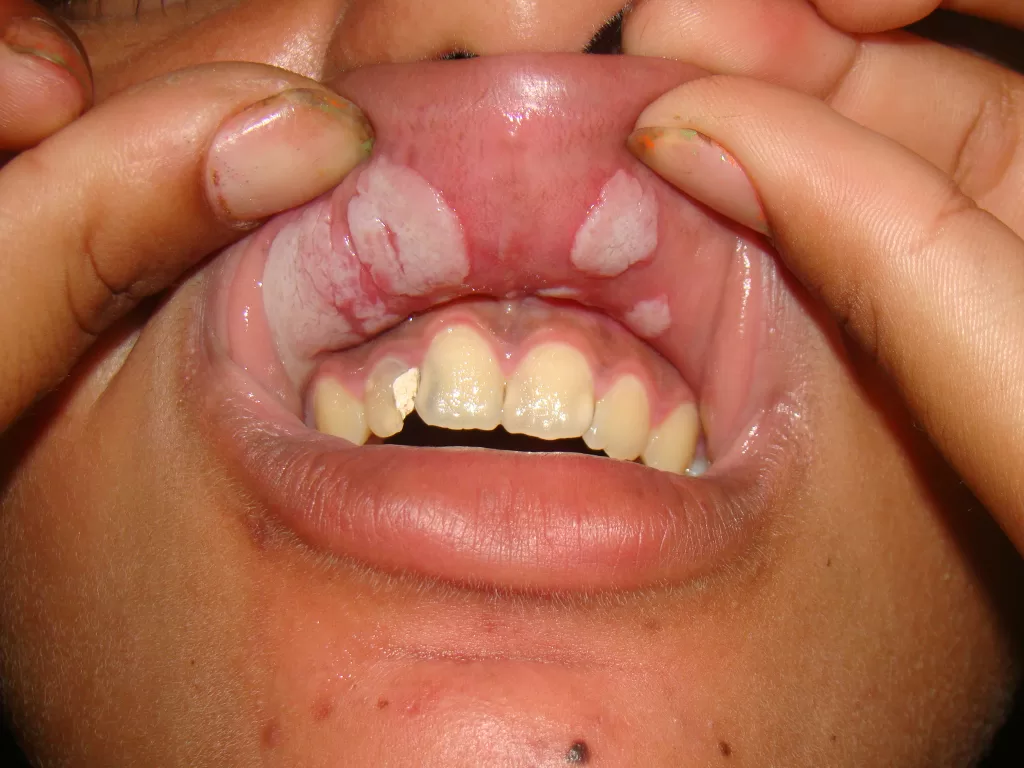
Localizações frequentes são o rosto, além do tronco e membros.
Lesões em Mucosas: mais frequente na boca, sendo potenciais transmissoras da doença via beijo.
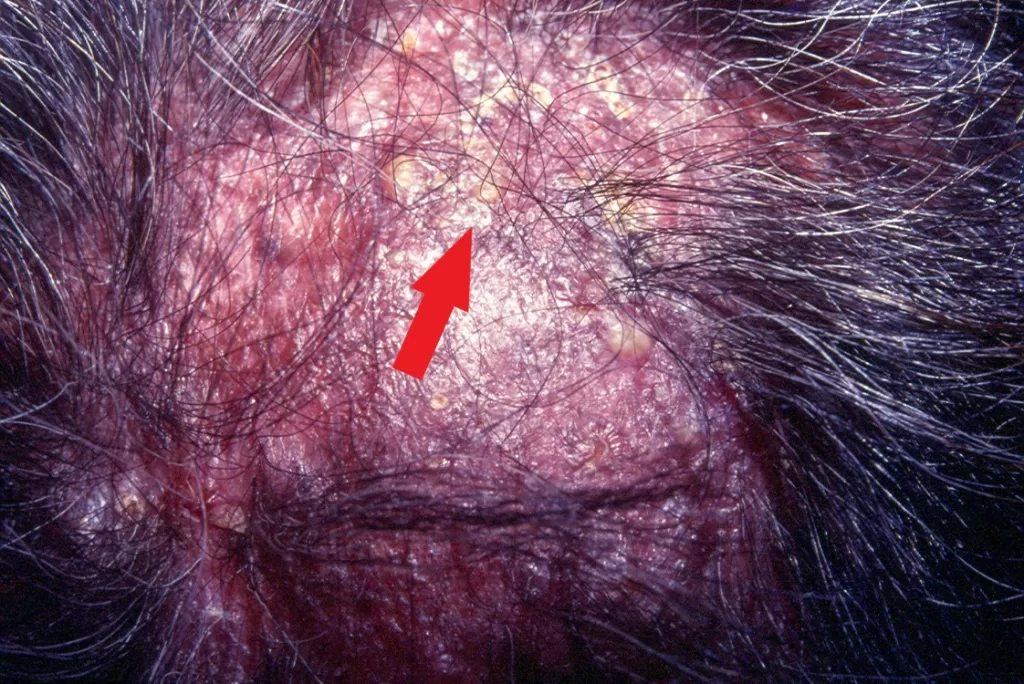
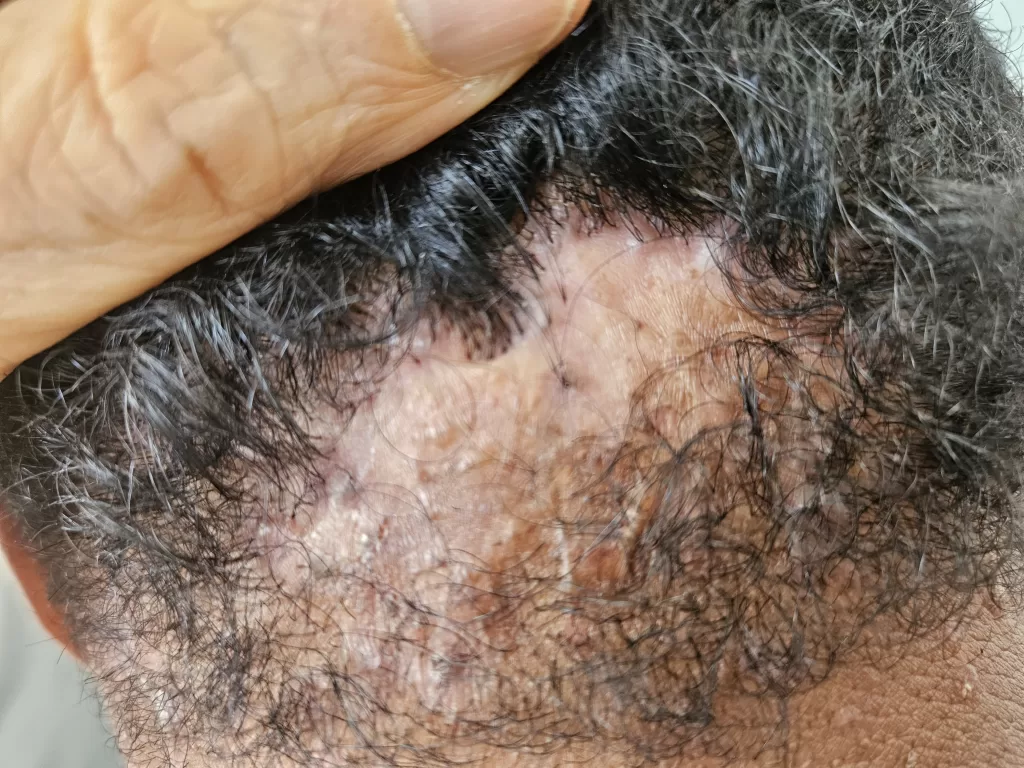
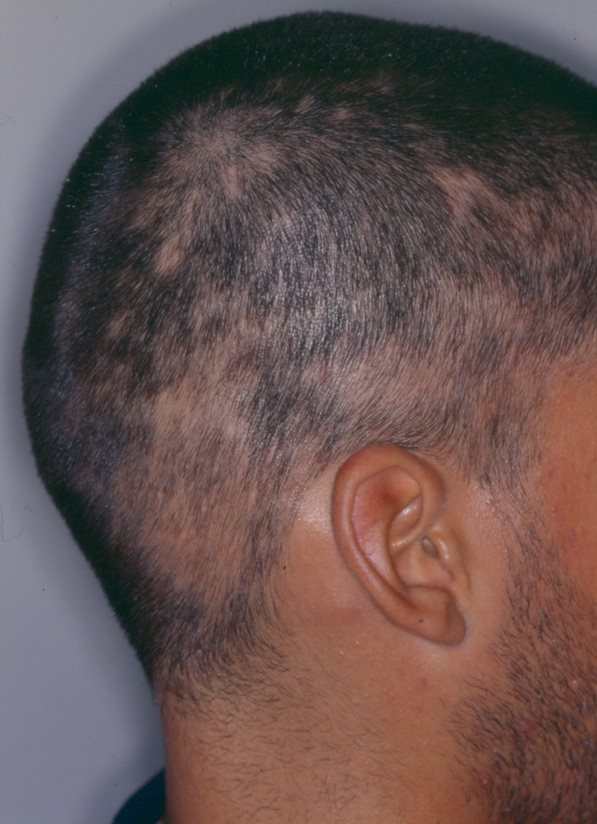
Alopecia: Queda de cabelo em áreas tipo “clareira”ou de maneira difusa.
Gânglios: Aumento de tamanho, perceptíveis ao toque, ocorrendo em 50 a 80% dos casos.
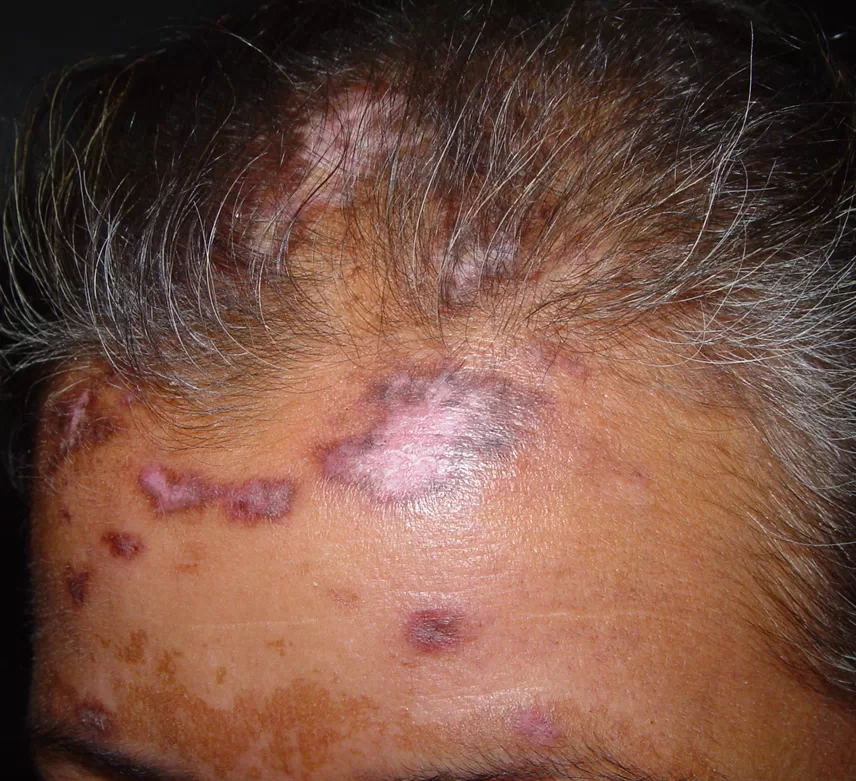
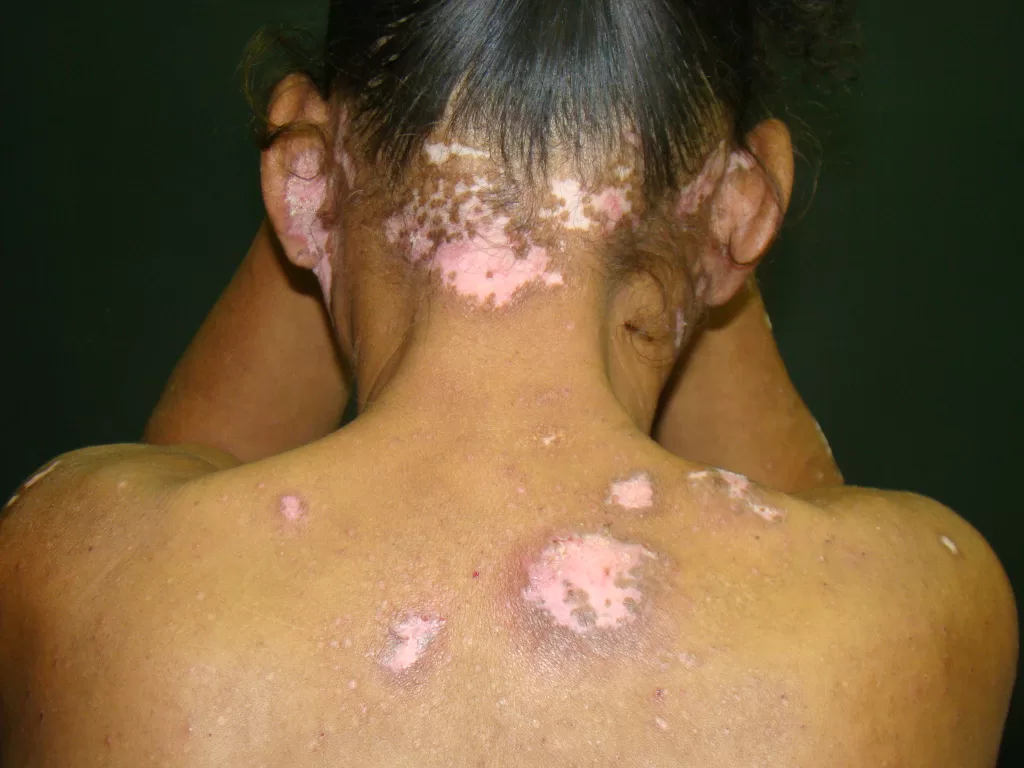
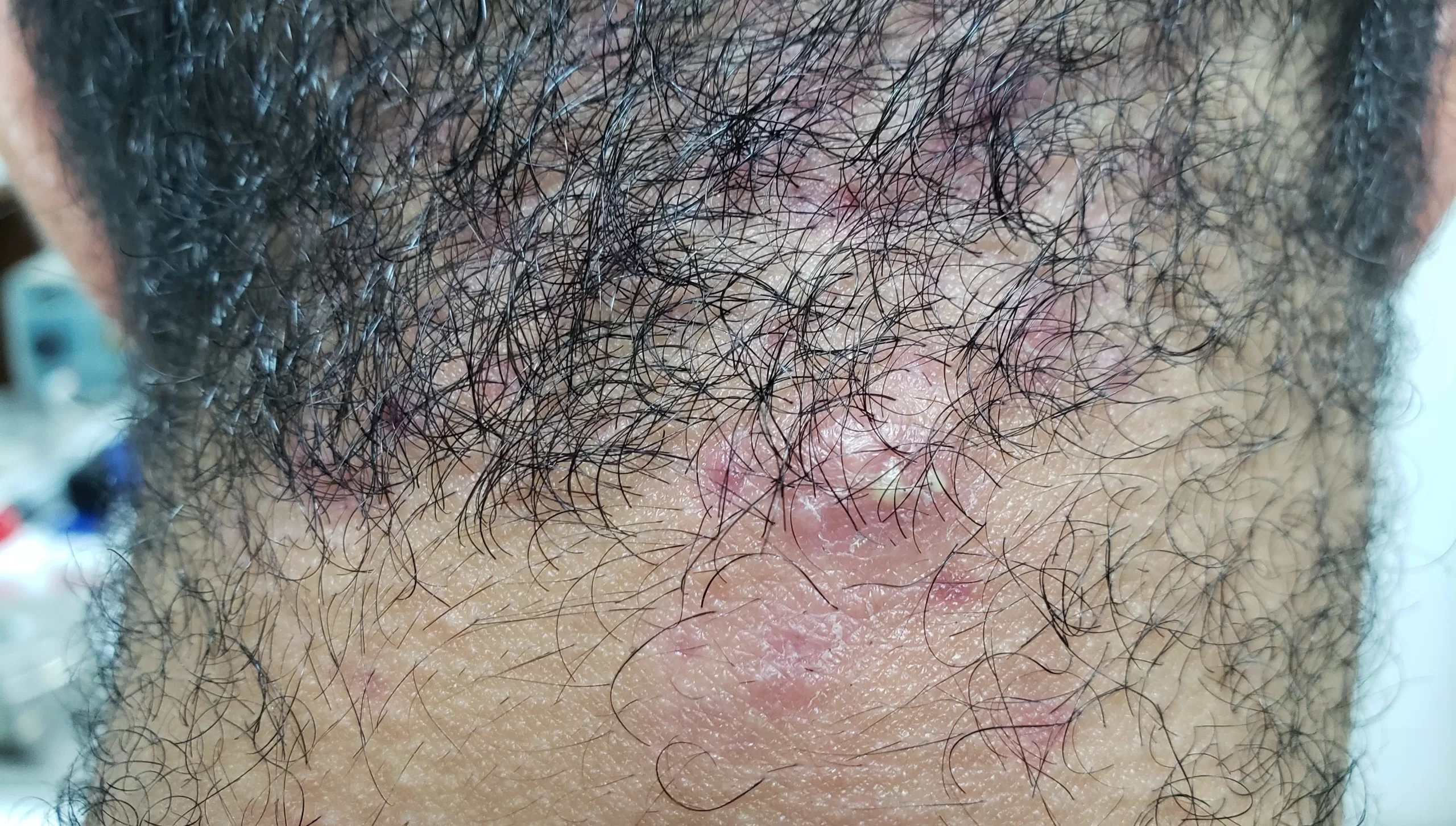
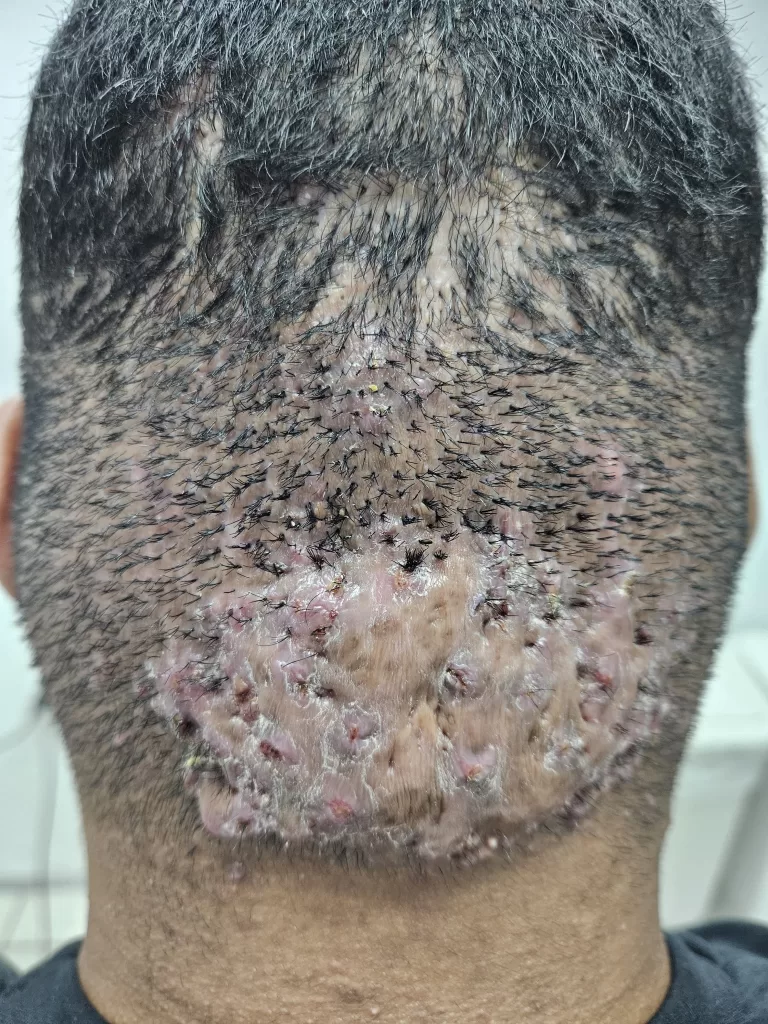
Sífilis Maligna Precoce: Sintomas e Características
A sífilis maligna precoce é uma forma rara da sífilis secundária. Era comum em pacientes desnutridos e debilitados e tem se manifestado com mais frequência em portadores de AIDS , nos tempos recentes.
Manifestações Clínicas da Sífilis Maligna Precoce:
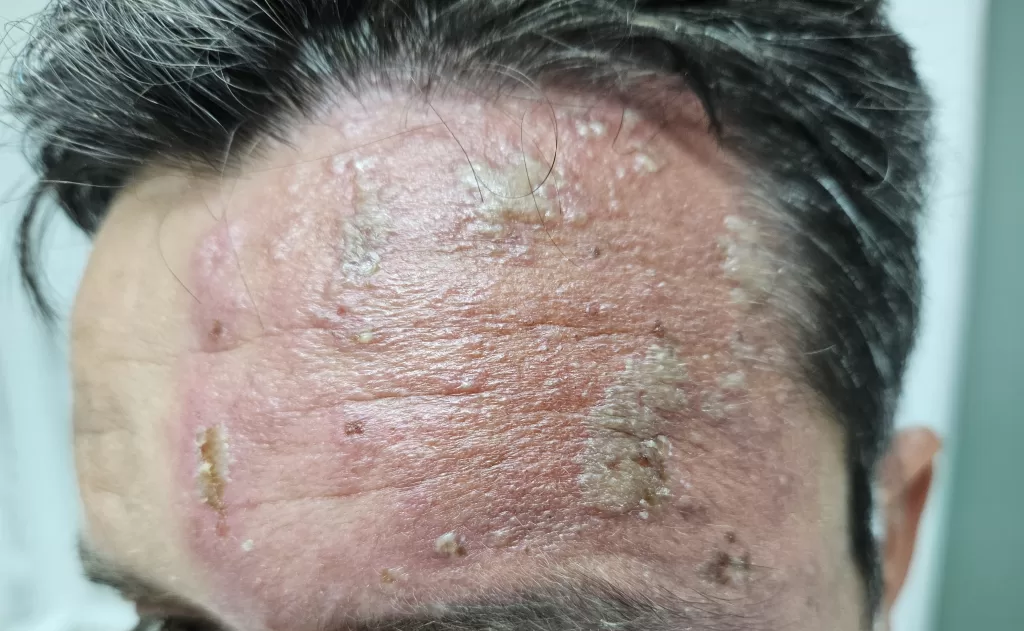
Lesões cutâneas:
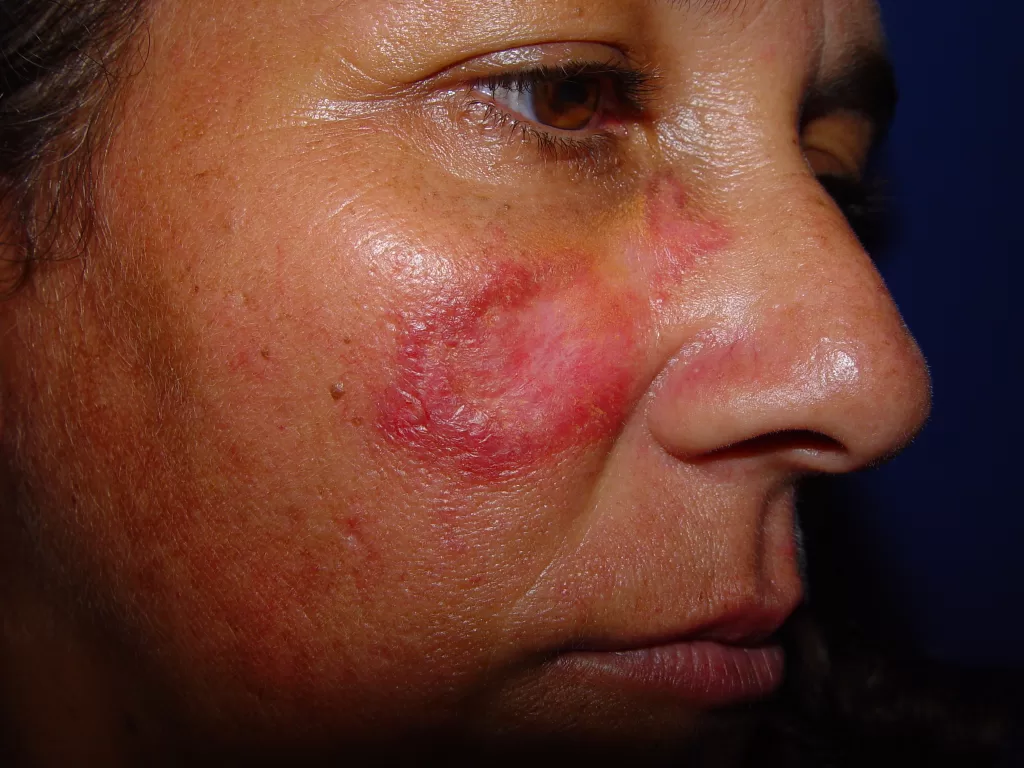
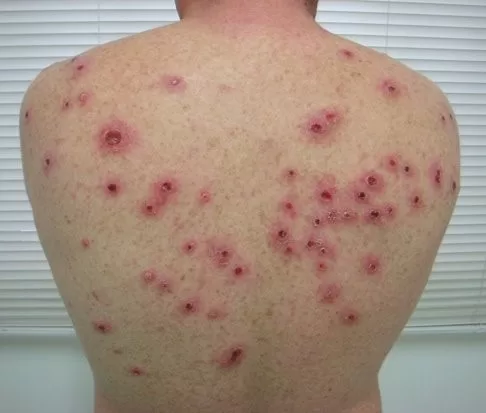
- Pápulas e pústulas variando de pequenas a grandes.
- Podem progredir para ulceração, gerando feridas cobertas por crostas.
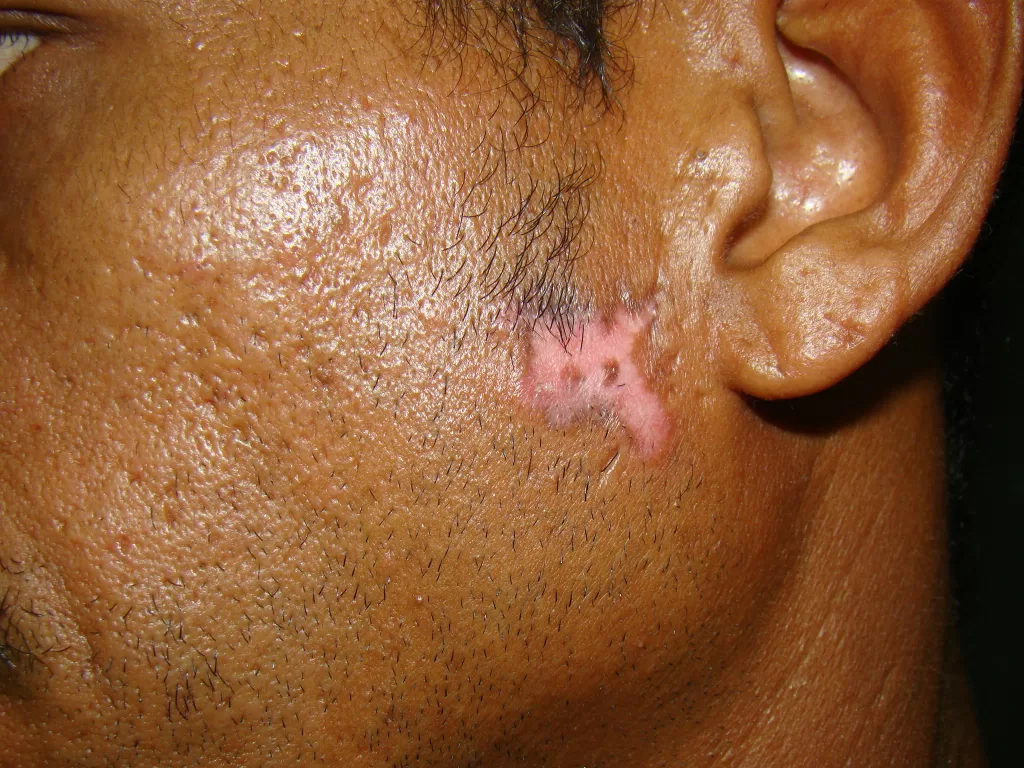
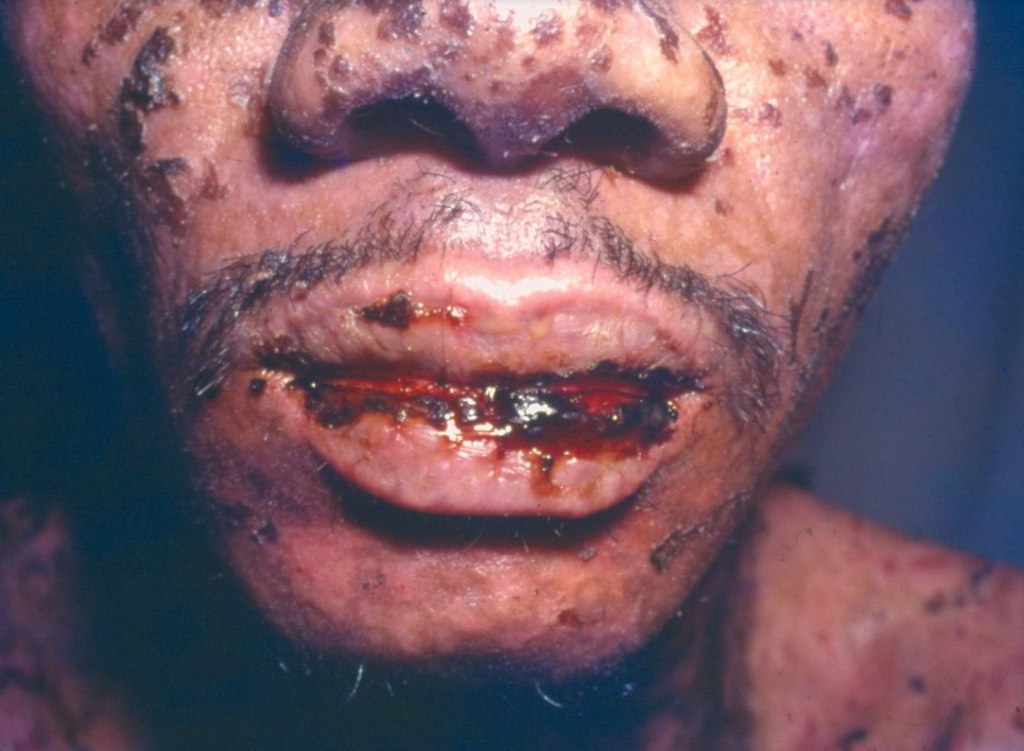
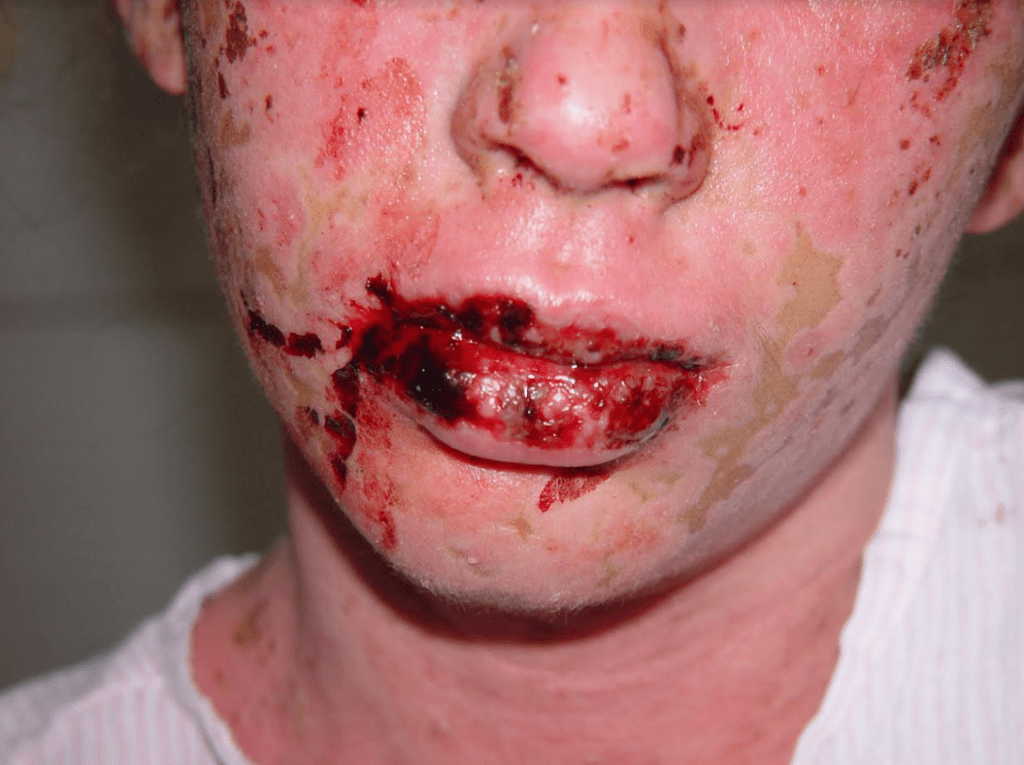
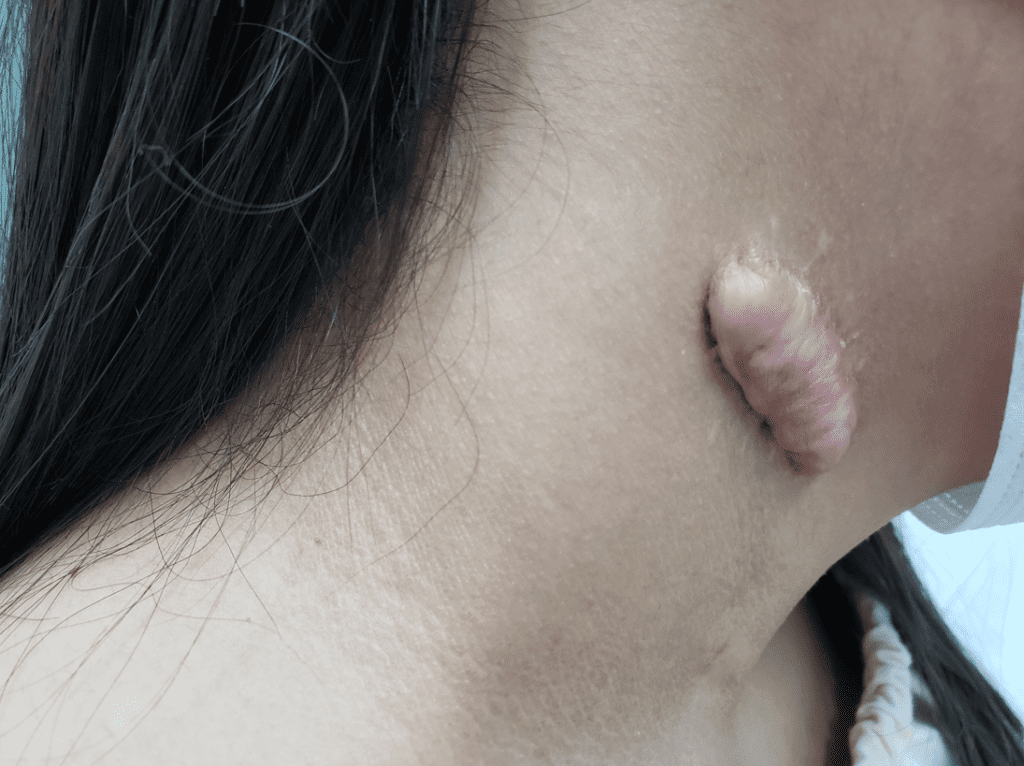
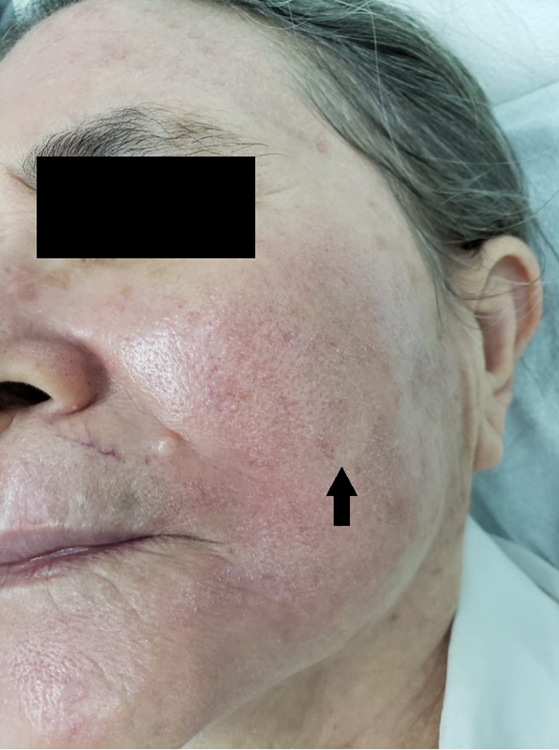
- As lesões são notavelmente mais profundas e destrutivas em comparação com outras variedades da sífilis secundária, levando à formação de cicatrizes (foto 13)
Localização:
- As lesões são frequentemente encontradas na cabeça, face e tórax.
Sintomas Associados:
- Febre
- Cefaleia (dor de cabeça)
- Artralgia (dor nas articulações)
Manifestações da Sífilis Secundária em Diferentes Órgãos
A sífilis secundária pode impactar vários órgãos, levando a diversas complicações. Aqui estão as manifestações mais comuns em diferentes órgãos.
- Baço:
- Aumento do tamanho do baço, condição conhecida como esplenomegalia.
- Fígado:
- Hepatite, indicando comprometimento hepático pela sífilis.
- Rins:
- Gera desenvolvimento da síndrome nefrótica .
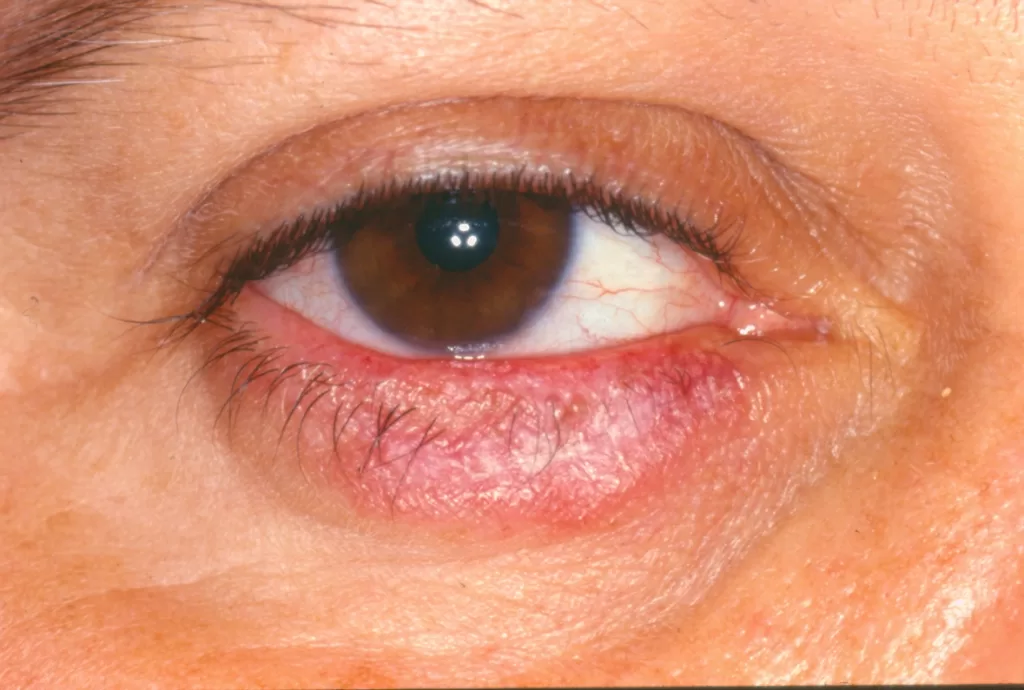
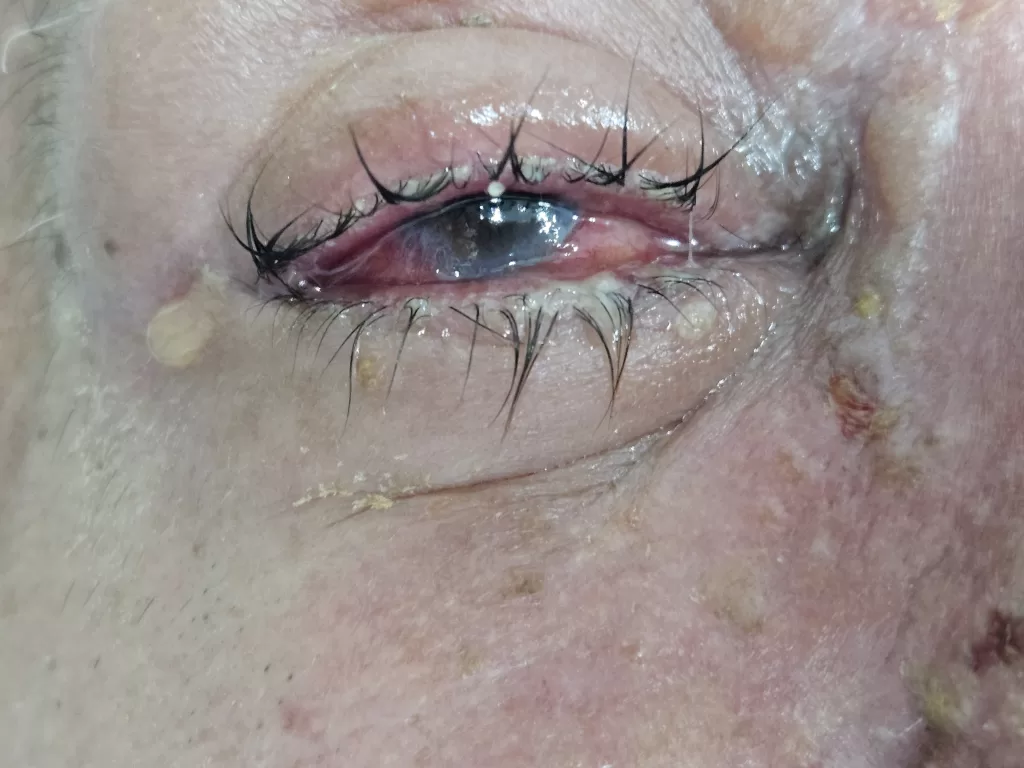
- Olhos:
- Condições oculares associadas incluem irite, iridociclite e uveítes anterior e posterior.
- Pode levar à diminuição da visão. É crucial tratar a sífilis prontamente, especialmente em pacientes com AIDS, para evitar a perda de visão.
- Audição:
- Comprometimento auditivo com diminuição da capacidade de ouvir.
Sífilis Tardia: Manifestações e Complicações
A sífilis tardia é uma fase da doença que se manifesta após um período de latência, podendo ocorrer de 1 a 30 anos após a fase secundária.
Esta fase é caracterizada por manifestações distintas na pele e no sistema cardiovascular.
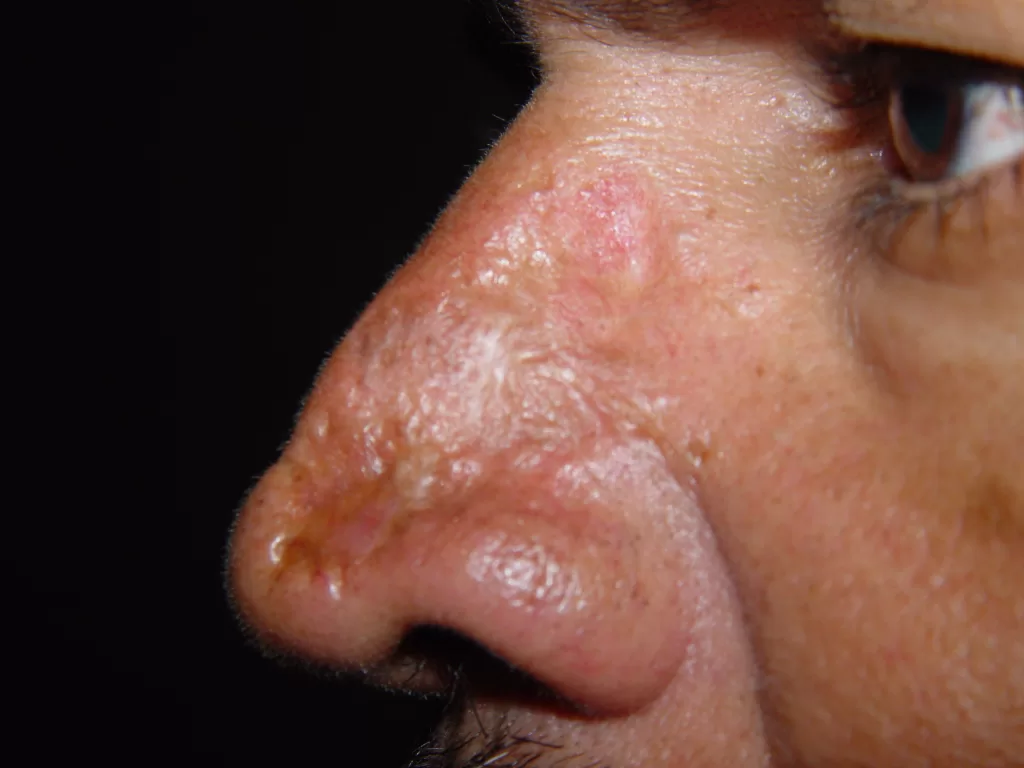
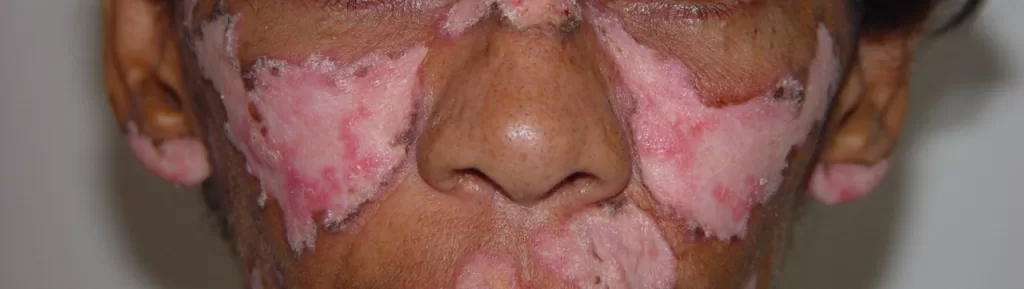
Manifestações Cutâneas da Sífilis Tardia:
As lesões de pele aparecem 2 a 7 anos após a fase secundária.
Caracterizam-se por serem reduzidas em número e agrupadas em áreas específicas.
Apresentam aspecto de tubérculos, nódulos e lesões em forma de arco e policíclicas (fotos 14, 15,16 e 17).
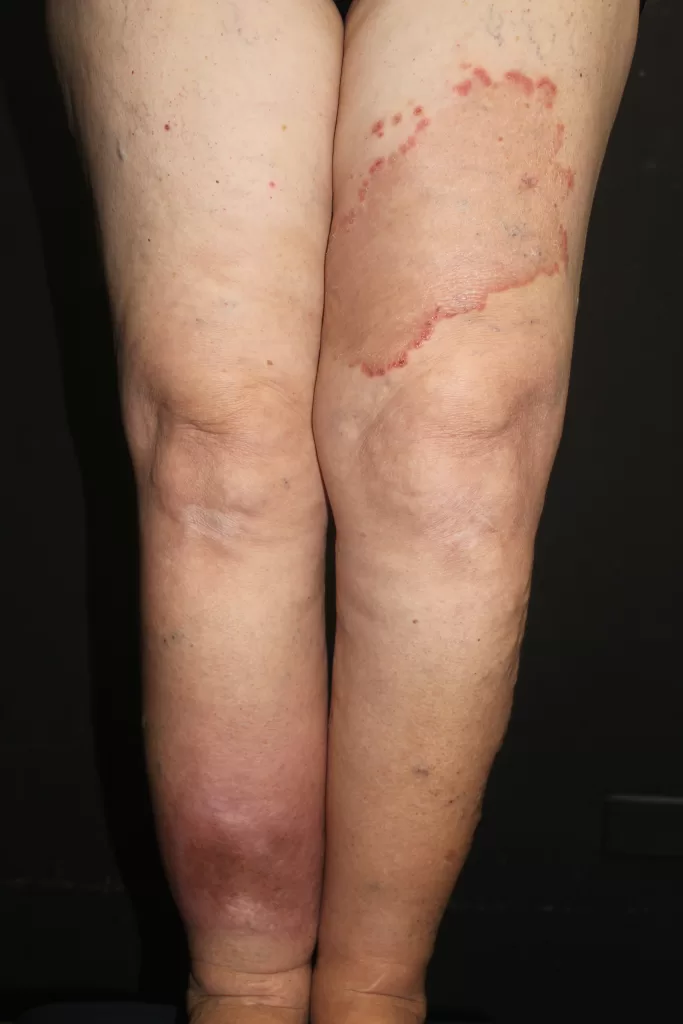
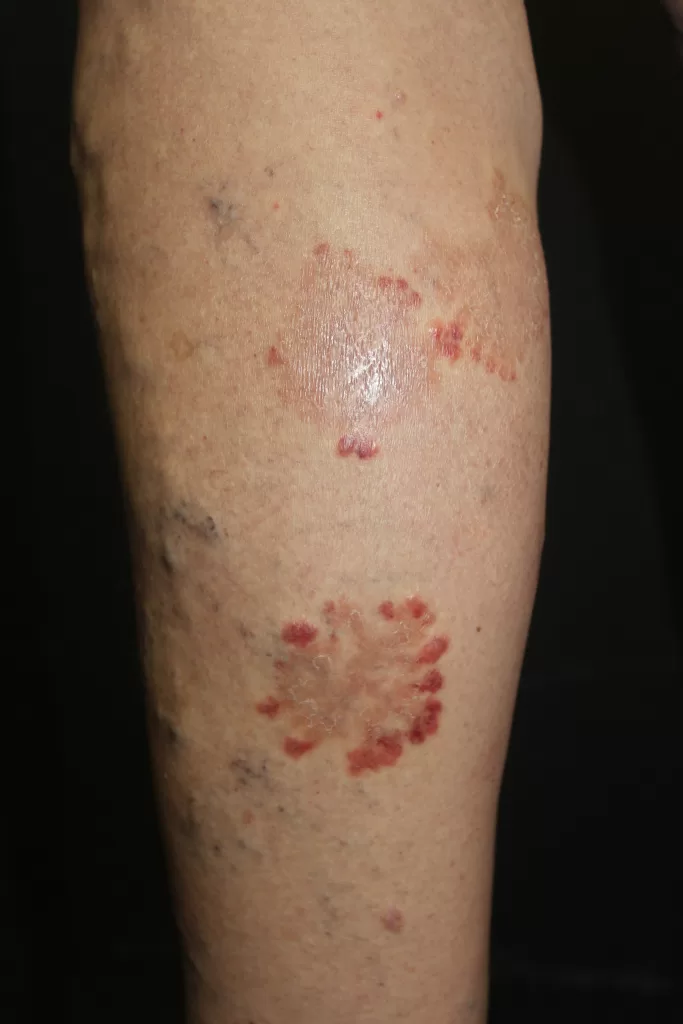
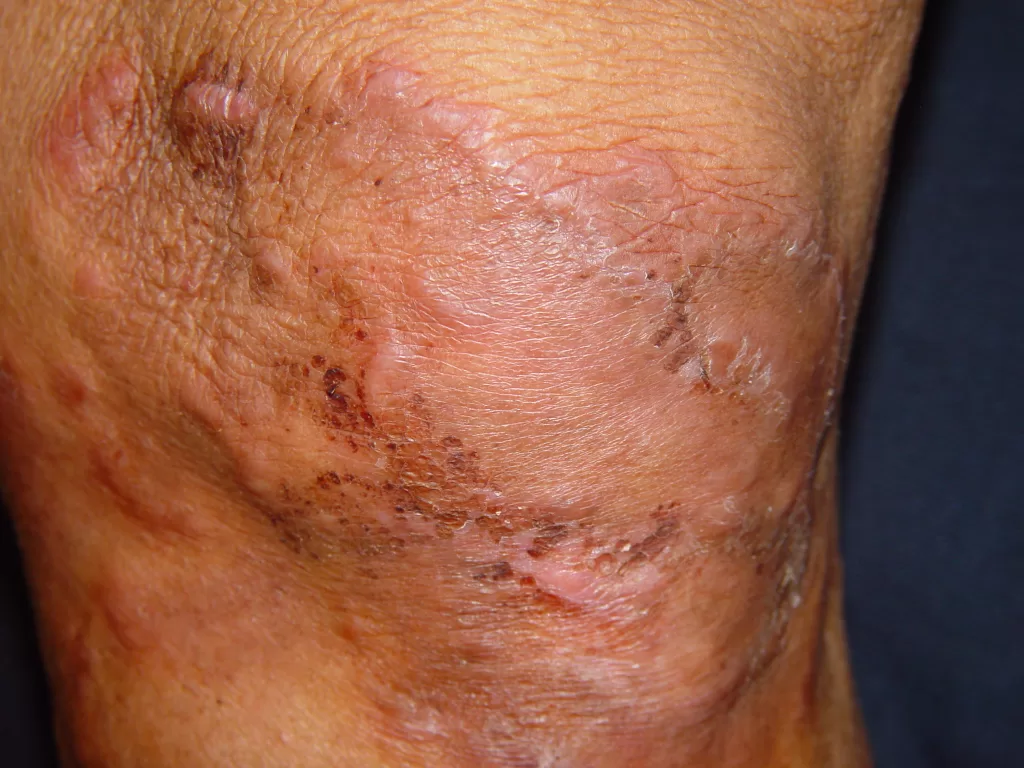
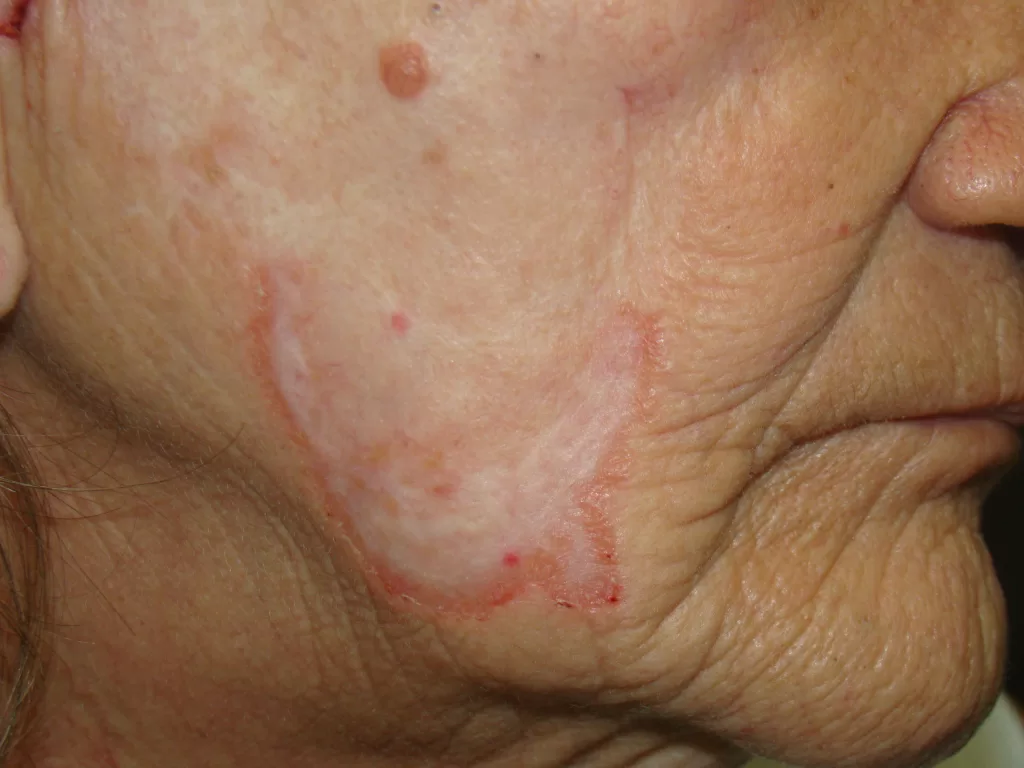
Evolução para gomas que amolecem e resultam em ulcerações profundas (foto 18).
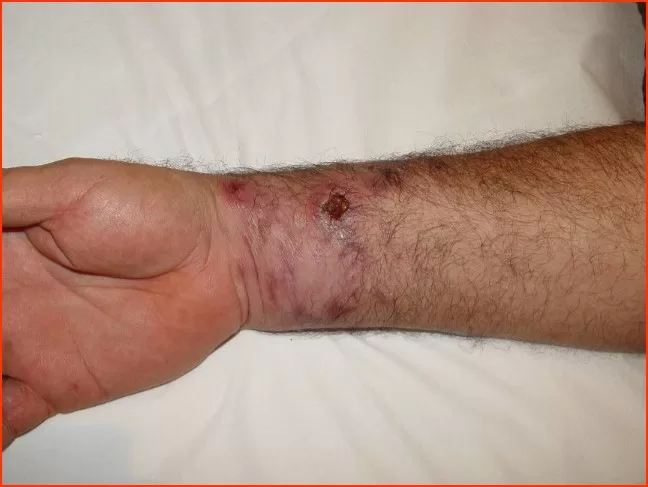
Localização no palato pode causar perfurações e refluxo de alimentos da boca para o nariz.
Lesões no rosto podem causar mutilação, inclusive impactando o nariz e olhos, chegando a causar cegueira.
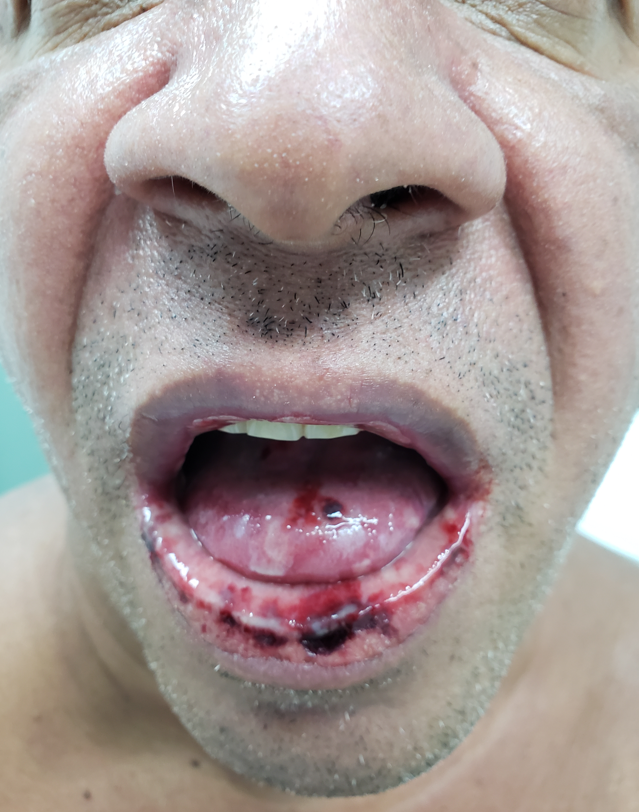
A língua pode ter aspecto esbranquiçado e ulcerado, podendo progredir para lesões pré-cancerosas.
Complicações Cardiovasculares da Sífilis Tardia:
- A aorta ascendente é frequentemente afetada, podendo resultar em insuficiência cardíaca, estenose das coronárias e aneurisma.
- Formação de “gomas” no coração pode causar lesões no septo entre os ventrículos, levando a arritmias cardíacas.
- Pode também afetar a parede livre do ventrículo esquerdo, causando aneurisma cardíaco.
Neurosífilis: Manifestações da Sífilis Tardia no Sistema Nervoso
A neurosífilis é uma complicação da sífilis tardia que afeta o sistema nervoso. Esta forma da doença impacta as meninges, (membranas que envolvem o cérebro) e resulta em diversos sintomas neurológicos.
Tabes Dorsalis: Resultado do comprometimento das meninges pela neurosífilis.
- Dificuldade para andar.
- Perda dos reflexos.
- Paralisia ocular.
- Surdez.
Paralisia Geral Progressiva: Uma forma avançada de neurosífilis , caracterizada por:
- Alterações comportamentais: incluindo agitação psicomotora, apatia, problemas de memória, irritabilidade, desvios de comportamento moral e social, e alienação completa.
- Insônia.
- Agitação psicomotora.
- Atrofia óptica com resultante diminuição da acuidade visual e campo visual.
Exames Laboratoriais para Diagnóstico de Sífilis
Pesquisa Direta do Treponema:
- Visão geral: Procura pela bactéria em locais específicos, como o cancro sifilítico e lesões da fase secundária.
- Método de destaque: Exame de campo escuro, que é considerado o mais preciso para identificar o treponema.
Provas Sorológicas
- Objetivo: Detectar anticorpos contra a bactéria, indicando sua presença.
- Quando se tornam positivas: Geralmente após 10-15 dias do surgimento do cancro.
- Importância: Cruciais durante a sífilis latente, fase em que a doença é identificável apenas por esses testes.
Tipos de Testes Sorológicos:
- Não Treponêmicos:
- VDRL: Amplamente usado para diagnóstico e monitoramento após o tratamento. Os níveis deste teste devem cair post-tratamento e são medidos regularmente para avaliar a eficácia do tratamento.
- Especificidade e Sensibilidade: O VDRL não é tão preciso quanto os testes específicos. A especificidade refere-se à prevenção de falsos negativos e a sensibilidade refere-se à detecção precoce da doença.
- Treponêmicos:
- Destaque: FTA-ABS: Popular devido à sua rapidez, facilidade e custo-benefício. No entanto, não é usado para avaliar a resposta ao tratamento. Uma vez positivo, pode permanecer assim mesmo após a cura, refletindo a presença de anticorpos protetores no corpo.
Tratamento
O método de tratamento para a sífilis varia conforme o avanço da doença.
Sífilis Recente (até 1 ano de duração):
- Penicilina Benzatina: Dose única de 2.400.000 UI por via intramuscular. É a escolha padrão para sífilis primária e secundária.
- Para pacientes alérgicos à penicilina:
- Doxiciclina: 100 mg, duas vezes ao dia, por 14 dias.
- Tetraciclina: 500 mg, quatro vezes ao dia, por 14 dias.
- Amoxicilina + Probenecid: 3 gramas de Amoxicilina com 500 mg de Probenecid, duas vezes ao dia, por 14 dias.
Sífilis Tardia (duração superior a 1 ano e sem acometimento do sistema nervoso):
- Penicilina Benzatina: Dose de 2.400.000 UI, uma vez por semana durante 3 semanas, totalizando 7.200.000 UI.
- Pacientes alérgicos à penicilina:
- Doxiciclina: 100 mg, duas vezes ao dia, por 28 dias.
Pacientes com Neurosífilis:
- Penicilina Cristalina: Dose diária de 24 milhões UI, intravenosa, durante 20 dias.
O tratamento efetivo da sífilis é crucial para prevenir complicações. É essencial seguir o regime de tratamento conforme a fase da doença e considerar possíveis alergias.